下列有关实验原理或操作正确的是
| A.SO2气体的还原性较强,不能使其通过浓硫酸干燥 |
| B.滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 |
| C.用图1装置吸收多余的HCl气体 |
| D.用图2装置检验溴乙烷发生消去反应生成乙烯 |

证某有机物属于烃,应完成的实验内容属是
A. 只测定它的C、H比
B. 只要证明它完全燃烧后产物只有H2O和CO2
C. 只测定其燃烧产物中H2O与CO2的物质量的比值
D. 测定该试样的质量及试样完全燃烧后生成CO2和H2O的质量
物质在氧气中完全燃烧后,生成物只有二氧化碳和水,以下说法正确的是
| A.该物质只含有碳元素和氢元素 |
| B.该物质只含有碳元素和氧元素 |
| C.该物质一定含有碳元素、氧元素、氢元素 |
| D.该物质一定含有碳元素和氢元素,可能含有氧元素 |
知天然气的主要成份CH4是一种会产生温室效应的气体,等物质的量的CH4和CO2产生的温室效应,前者大。下面是有关天然气的几种叙述:①天然气与煤、柴油相比是较清洁的能源;②等质量的CH4和CO2产生的温室效应也是前者大;③燃烧天然气也是酸雨的成因之一。其中正确的
| A.是①、②、③ | B.只有① | C.是①和② | D.只有③ |
2005年4月22日是第36个“世界地球日”,我国国土资源部确定今年“世界地球日”的主题为“善待地球——科学发展,构建和谐”。中国邮政并发行了纪念邮票。下列行为不符合活动主题的是
| A.开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料 |
| B.控制含磷洗涤剂的使用,防止水体富菅养化,保护水资源 |
| C.更新采煤、采油技术,提高产量以满足工业生产的快速发展 |
| D.落实资源的“3R”发展观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle) |
2010年上海世博会,上海将有千辆氢燃料电池车上路,参看某种氢燃料电池原理图,下列说法不正确的是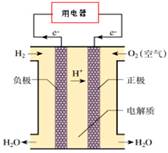
| A.氢氧燃料电池是一种具有应用前景的绿色电源 |
| B.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
| C.氢燃料电池能量转换率比氢气直接燃烧高 |
| D.氢燃料电池工作时,发出淡蓝色火焰 |