下列晶体中不属于原子晶体的是()
| A.干冰 | B.金刚砂 | C.金刚石 | D.水晶 |
下列各组中都属于分子晶体的是()
| A.碘、二氧化碳、白磷、C60 | B.食盐、二氧化碳、白磷、二氧化硅 |
| C.SO2、金刚石、N2、铜 | D.醋酸、甲烷、石墨、氧化钠 |
设NA为阿伏加德罗常数。如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是()
A.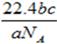 |
B.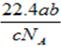 |
C.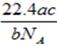 |
D. |
将2.3克钠投入W克水中,所得溶液中Na+与水分子个数之比1:100,溶液密度为1.2g.ml-1,下列有关说法不正确的是()
| A.W=181.8 |
| B.此过程中,水被还原,共得到0.1NA个电子 |
| C.所得溶液中溶质质量分数约为2.174% |
| D.仅据上述条件无法求算所得溶液的物质的量浓度 |
同温同压下,在两个密闭容器中分别充有质量相同的甲、乙两种气体,且甲的密度大于乙的密度。则下列说法正确的是()
| A.甲的物质的量比乙的物质的量少 |
| B.甲气体所占体积比乙气体所占体积大 |
| C.甲相对分子质量比乙相对分子质量小 |
| D.甲气体摩尔体积比乙气体摩尔体积小 |