已知反应A(g)+3B(g)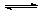 2C(g)+D(g)在某段时间内以A的浓度变化表示的化学反应速率为 1 mol·L-1·min-1,则此段时间内以C的浓度变化表示的化学反应速率为
2C(g)+D(g)在某段时间内以A的浓度变化表示的化学反应速率为 1 mol·L-1·min-1,则此段时间内以C的浓度变化表示的化学反应速率为
| A.0.5 mol·L-1·min-1 | B.1 mol·L-1·min-1 |
| C.2 mol·L-1·min-1 | D.3 mol·L-1·min-1 |
某同学利用家中废旧材料制作一个可使玩具扬声器发出声音的电池,装置如图所示。下列说法正确的是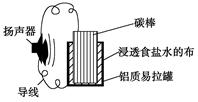
| A.碳棒上发生的主要反应为:2H++2e-=H2↑ |
| B.铝质易拉罐将逐渐得到保护 |
| C.电池总反应为:4Al+3O2+6H2O==4Al(OH)3 |
| D.电子方向为:铝质易拉罐→导线→扬声器→导线→碳棒→浸透食盐水的布 |
有关能量的判断或表示方法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 |
| B.从C(石墨)==C(金刚石) ΔH=+1.19 kJ·mol-1,可知:金刚石比石墨更稳定 |
| C.由H+(aq)+OH-(aq)==H2O(l) ΔH=-57.3 kJ·mol-1,可知:含0.5 mol H2SO4的浓溶液与含1 molNaOH的溶液混合,放出热量大于57.3 kJ |
| D.2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ·mol-1 |
用1 mol·L-1NaOH溶液中和某浓度的硫酸溶液时,其pH和所加NaOH溶液的体积关系如图所示,原硫酸溶液的物质的量浓度和反应后溶液的总体积分别是
| A.0.5 mol·L-1 100 mL | B.0.5 mol·L-180 mL |
| C.1 mol·L-160 mL | D.1 mol·L-180 Ml |
下列关于化学反应的熵变的叙述中,正确的是
| A.化学反应的熵变与反应的方向无关 |
| B.化学反应的熵变直接决定了反应的方向 |
| C.熵变为正的反应都是混乱度增大的反应 |
| D.能自发进行的反应熵变一定都为正 |
下列事实中不能用勒夏特列原理来解释的是
| A.向H2S水溶液中加入NaOH固体有利于S2-增多 |
| B.鼓入过量空气有利于SO2转化为SO3 |
| C.高压对合成氨有利 |
| D.500 ℃左右比室温更有利于氨的合成 |