在密闭容器中,反应X2(g) +Y2(g) 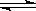 2XY(g);△H < 0,达到平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是.( )
2XY(g);△H < 0,达到平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是.( )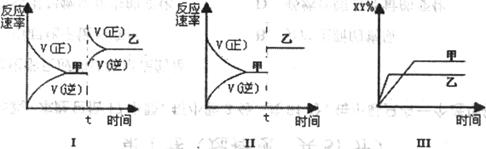
| A.图I是加入适当催化剂的变化情况 |
| B.图II是扩大容器体积的变化情况 |
| C.图III是增大压强的变化情况 |
| D.图III是升高温度的变化情 |
t℃时,将100 g某物质A的溶液蒸发掉10 g水,恢复至t℃,析出2.5 g晶体;再蒸发掉10 g水,恢复至t℃,析出7.5 g晶体。下列说法中正确的是
| A.t℃时原溶液是饱和溶液 | B.t℃时A的溶解度为75 g |
| C.若A是CuSO4,则7.5 g晶体中含水2.7 g | D.原溶液中A的质量分数为40% |
硫酸铵在加强热条件下分解,生成氨、二氧化硫、氮气和水。反应中生成的氧化产物和还原产物的物质的量之比是
| A.1:3 | B.2:3 | C.1:1 | D.4:3 |
FeCl2溶液中混有FeI2杂质,根据已知反应:①2FeCl3+2KI=2FeCl2+2KCl+I2;②2FeCl2+Cl2=2FeCl3;③F2+2KI(固)=2KF+I2中的有关事实,要除去其中的FeI2,应选用的试剂是
| A.F2 | B.过量Cl2 | C.FeCl3 | D.FeCl2 |
将标准状况下,将VL A气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此 溶液的物质的量浓度(mol/L)为
溶液的物质的量浓度(mol/L)为
A. |
B. |
C. |
D.100VρM /(MV+2240) |
两种金属粉末的混合物12g,投入足量的稀硫酸中,在标准状况下产生11.2 L气体,则这种混合物可能是
| A.Zn、Al | B.Fe、Zn | C.Al、Mg | D.Mg、Cu |