某化合物由碳、氢、氧三种元素组成,红外光谱图显示有三种共价键的振动吸收,核磁共振氢谱图显示有三个峰,峰面积比为6 :1:1,则该有机物的结构简式是
:1:1,则该有机物的结构简式是
A.C2 H5OCH3 H5OCH3 |
B.CH3CH(OH)CH3 | C.CH3CH2CH2OH | D.CH3CH2CHO |
下列各组离子能在指定的环境下可以大量共存的是
| A.在pH=0的溶液中:Na+、Fe2+、Cl-、NO3- |
| B.由水电离出的c(H+)=1×10-14 mol·L-1的溶液:K+、NH4+、Cl-、CO32- |
| C.c(H+)<c(OH-)溶液:Na+、K+、SO32-、AlO2- |
| D.某无色透明溶液:Na+、Al3+、SO42-、HCO3- |
下列与滴定实验有关的说法中正确的是
| A.用NaOH滴定盐酸时,只能用酚酞作指示剂 |
| B.用KMnO4滴定亚硫酸钠溶液的实验中不需要另外加入指示剂 |
| C.用滴定管准确量取20.0 mL盐酸 |
| D.用NaOH滴定盐酸时,若滴定结束时俯视刻度,会导致测定结果偏高 |
下列叙述正确的是(用NA代表阿伏加德罗常数的值)
| A.1 mol·L-1NaCl溶液含有NA个Na+ |
| B.1 L 0.1 mol·L-1氨水含有0.1 NA个OH- |
| C.电解饱和食盐水若产生2 g氢气,则转移2 NA个电子 |
| D.将0.1 mol氯化铝溶于1 L水中,所得溶液含有0.1 NA个Al3+ |
下列有关电离或离子方程式中,正确的是
A.将饱和FeCl3溶液滴入沸水中制备胶体:Fe3++3H2O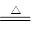 Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
| B.用FeS去除废水中的Hg2+:Hg2+ + S2-=== HgS↓ |
C.用惰性电极电解MgCl2溶液: 2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
D.KHS溶液中HS-的电离:HS-+ H2O  H3O+ + S2- H3O+ + S2- |
水的电离过程为H2O H++OH—,在不同温度下其平衡常数为Kw (25℃)=1.0×10-14,Kw (35℃)=2.1×10-14。则下列叙述正确的是
H++OH—,在不同温度下其平衡常数为Kw (25℃)=1.0×10-14,Kw (35℃)=2.1×10-14。则下列叙述正确的是
| A.水的电离是一个放热过程 |
| B.35℃时,c(H+)>c(OH-) |
| C.25℃时,pH=3的盐酸中由水电离产生的c(OH-)=1.0×10-3mol/L |
| D.25℃时,向溶液中加入稀氨水,平衡逆向移动,Kw不变 |