时钟反应或振荡反应提供了迷人课堂演示实验,也是一个活跃的研究领域。测定含有I—浓度很小的碘化物溶液时,利用振荡反应进行化学放大,以求出原溶液中碘离子的浓度。主要步骤如是:
①在中性溶液中,用溴将试样中I-氧化成IO3-,将过量的溴除去。
②再加入过量的KI,在酸性条件下,使IO3-完全转化成I2。
③将②中生成的碘完全萃取后,用肼将其还原成I-,方程式为:N2H4+2I2=4I-+N2+4H+
④将生成的I-萃取到水层后用①法处理。
⑤将④得到的溶液加入适量的KI溶液,并用硫酸酸化。
⑥将⑤反应后的溶液以淀粉作指示剂,用Na2S2O3标准溶液滴定,方程式为:
2Na2S2O3+I2 Na2S4O6+2NaI经过上述放大后,溶液中I-浓度放大为原溶液中I-浓度的(设前后溶液体积相等)
Na2S4O6+2NaI经过上述放大后,溶液中I-浓度放大为原溶液中I-浓度的(设前后溶液体积相等)
| A.2倍 | B.4倍 | C.36倍 | D.6倍 |
密闭容器中反应:aX(g)+bY(g)⇌cZ(g)+dW(g),反应达平衡后,保持温度不变,将气体压缩到原来的一半体积,当再次达到平衡时,W的浓度为原平衡的1.8倍.下列不正确的是
| A.a+b>c+d | B.平衡向逆反应方向移动 |
| C.Z的体积分数减小 | D.X的转化率下降 |
已知反应:2NO2 (g)⇌N2O4(g),把NO2、N2O4的混合气体盛装在两个连通的烧瓶里,然后用止水夹夹住橡皮管,把烧瓶A放入热水里,把烧瓶B放入冰水里,如图所示.与常温时烧瓶内气体的颜色进行对比发现,A烧瓶内气体颜色变深,B烧瓶内气体颜色变浅.下列说法错误的是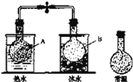
A.上述过程中,A烧瓶内正、逆反应速率均加快
B.上述过程中,B烧瓶内c(NO2)减小,c(N2O4)增大
C.上述过程中,A、B烧瓶内气体密度均保持不变
D.反应2NO2(g)⇌N2O4(g)的逆反应为放热反应
在一定温度下将lmol CO(g)和lmol H2O(g)通入一个容积固定的密闭容器中反应:CO(g) +H2O(g) CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g),当再次达到平衡后,CO2的物质的量可能是
CO2(g)+H2(g),达到平衡后CO2的物质的量为0.6mol,再通入4molH2O(g),当再次达到平衡后,CO2的物质的量可能是
| A.n(CO2)="0.6" mol |
| B.n(CO2)="1" mol |
| C.1 mol<n(CO2)<4 mol |
| D.0.6 mol<n(CO2)<1 mol |
在体积固定的密闭容器中加入2 mol A和1 mol B,发生反应:2A(g)+B(g)⇌3C(g)+D(g),达到平衡时C的浓度为a mol/L.若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为a mol/L的是
| A.4mol A+2mol B |
| B.2mol A+1mol B+3mol C+1mol D |
| C.3mol C+1mol D+1mol B |
| D.3mol C+1mol D |
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH- (aq)=H2O(l);△H= -57.3kJ/mol。向lL 0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时,反应热△H1、△H2、△H3的关系正确的是
| A.△ H1>△ H2>△ H3 | B.△ H2>△ H3>△ H1 |
| C.△ H1>△ H3>△ H2 | D.△ H3>△ H2>△ H1 |