钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层 四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加
四氧化三铁的技术过程。其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加 热到130℃反应。其过程可以用如下化学方程式表示
热到130℃反应。其过程可以用如下化学方程式表示
①3Fe+NaNO2+5NaOH===3Na2FeO2+H2O+NH3↑
②6Na2FeO2+NaNO2+5H2O===3Na2Fe2O4+NH3↑+7NaOH
③Na2FeO2+Na2Fe2O4+2H2O===Fe3O4+4NaOH
下列说法正确的是
| A.反应①不是氧化还原反应 |
| B.该生产过程不产生任何污染 |
| C.整个反应过程中,每有5.6 g Fe参加反应转移0.8 mol电子 |
| D.反应②中的氧化剂是NaNO2 |
醋酸溶液中滴入稀氨水,溶液的导电能力发生变化,其电流I随加入氨水的体积V的变化曲线图是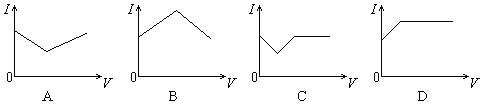
某酸溶液中C(H+)=0.1mol·L-1,则该酸溶液的物质的量浓度()
| A.一定等于0.1mol·L-1 | B.一定大于0.1mol·L-1 |
| C.一定小于0.1mol·L-1 | D.无法确定 |
氨水中所含有的分子和离子有()
①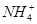 ②H2O③NH3④NH3·H2O⑤H+⑥OH-
②H2O③NH3④NH3·H2O⑤H+⑥OH-
| A.①②③ | B.①②③④⑤⑥ | C.②③④⑤⑥ | D.②③④⑤ |
全球变暖给我们敲响了警钟,地球正面临巨大的挑战.下列说法不正确的是()
| A.推广“低碳经济”,减少温室气体的排放 |
| B.利用晶体硅制作的太阳能电池可将太阳能直接转化为电能 |
| C.推广“绿色自由”计划,吸收空气中的CO2并利用廉价能源合成汽油 |
| D.推进小火力发电站的兴建,缓解地方用电困难,促进地方经济的快速发展 |
已知:①向KMnO4固体中滴加浓盐酸,产生黄绿色气体(Cl2);
②向FeCl2溶液中通入少量①产生的气体,溶液变为棕黄色;
③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。
下列判断正确的是( )
| A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2 |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验①生成的气体不能使湿润淀粉KI试纸变蓝 |
| D.实验②证明Fe2+既有氧化性又有还原性 |