某温度下,反应H2(g)+I2(g)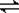 2HI(g)的正反应为放热反应,在带有活塞的密闭容器中达到平衡。下列说法中正确的是( )
2HI(g)的正反应为放热反应,在带有活塞的密闭容器中达到平衡。下列说法中正确的是( )
| A.体积不变,升温,正反应速率减小 |
| B.温度、压强均不变,充入HI气体,开始时正反应速率增大 |
| C.温度不变,压缩气体的体积,平衡不移动,颜色加深 |
| D.体积、温度不变,充入氮气后,正反应速率将增大 |
下列制备和收集气体的实验装置合理的是
下列说法不正确的是
① CO2分子的比例模型示意图:
②-OH与 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同
③HCN分子的结构式:H-C≡N;
④NaHCO3在水中的电离方程式:NaHCO3 Na++H++CO32-;
Na++H++CO32-;
⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;
⑥铝既能与盐酸反应又能与NaOH溶液反应,故铝是两性元素;
⑦风化、干馏、裂化都是化学变化
| A.①②⑤ | B.③④⑦ | C.①④⑥ | D.④⑤⑥ |
化学与生产、生活密切相关。下列叙述中,不正确的是
①制作计算机芯片的材料是Si晶体,漂白液的有效成分是NaClO
②二氧化碳和氮气均是造成温室效应的气体
③食醋可去除水垢,NH4Cl溶液可去除铁锈
④SO2和NO2都能使雨水的pH < 5.6,造成酸雨
⑤硅胶可用作食品干燥剂
⑥向FeCl3溶液中不断加入NaOH溶液制备Fe(OH)3胶体
⑦用铜粉和硫粉混合加热制备CuS
⑧向铝盐溶液中不断滴入烧碱溶液制备Al(OH)3
| A.②③⑦ | B.②⑥⑦⑧ | C.②③⑦⑧ | D.①②③⑥⑧ |
分子式为C5H8O2的有机物,能使溴的CCl4溶液褪色,也能与NaHCO3溶液反应生成气体,则符合上述条件的同分异构体(不考虑立体异构)最多有
| A.5种 | B.6种 | C.7种 | D.8种 |
某化合物由两种单质直接反应生成,将其加(通)入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是
| A.SO3 | B.HCl | C.FeCl2 | D.Na2O2 |