同系物具有:①相同的通式;②相同的最简式;③相同的物理性质;④相似的化学性质
| A.①②④ | B.①④ | C.①③④ | D. ①②③ ①②③ |
下列反应的离子方程式,书写正确的是
A.钠跟水反应 |
B.溶液中加入过量氨水 |
C.硫酸和氢氧化钡溶液反应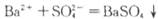 |
D.大理石跟盐酸反应放出气体 |
关于相同质量的O2和O3的说法一定正确的是
| A.分子数之比为1:1 |
| B.原子数之比为1:1 |
| C.体积之比3:2 |
| D.物质的量之比2:3 |
下列各组离子因发生氧化还原反应而不能大量共存的是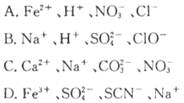
将饱和溶液FeCl3加入沸水中能制得Fe(OH)3胶体,下列有关说法正确的是
| A.溶液和胶体的本质区别是能否发生丁达尔效应 |
| B.含0.1 mol FeCl3溶质的溶液形成胶体后,胶体粒子为0.1 mol |
| C.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| D.可通过观察液体是否澄清透明,来区别溶液和胶体 |
N0为阿伏加德罗常数的值,下列叙述正确的是
| A.1 mol CO2中含有原子数N0 |
| B.1 L 1mol/L的硫酸钠溶液中,所含Na+数为N0 |
| C.标准状况下,11.2 L水所含分子数为0.5 N0 |
| D.在反应中,1 mol Fe和足量盐酸反应失去的电子数为2 N0 |