下列各组气态氢化物中,按稳定性顺序排列正确的是
| A.SiH4> PH3>H2S>HCl | B.HF>HCl>HBr>HI |
| C.NH3>PH3>AsH3>HF | D.PH3>AsH3> H2S>HCl |
若用x代表一个中性原子中核外的电子数,y代表此原子的原子核内的质子数,z代表此原子的原子核内的中子数,则对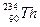 的原子来说()
的原子来说()
| A.x="90" y="90" z="234" | B.x="90" y="90" z=144 |
| C.x="144" y="144" z="90" | D.x="234" y="234" z=324 |
下列叙述中的非金属元素,其氢化物最稳定的是()
| A.构成矿物和岩石的主要元素 | B.空气中含量最多的元素 |
| C.单质在常温下是液态的元素 | D.地壳中含量最多的元素 |
下列说法错误的是()
| A.作半导体材料的元素大多数位于周期表中金属和非金属的交界处 |
| B.农药中常含有的元素通常在元素周期表的右上方区域内 |
| C.作催化剂材料的元素通常在元素周期表的左下方区域内 |
| D.在周期表过渡元素第ⅢB族到ⅥB族中,可寻找到耐高温和耐腐蚀的合金材料 |
下列化学用语表述正确的是()
A.Cl-的结构示意图 |
B.MgCl2的电子式 |
C.CCl4的结构式 |
D.高碘酸的分子式 H4IO5 |
X、Y、Z三种元素的电子层数相同,它们的最高价氧化物分别为酸性氧化物、碱性氧化物、两性氧化物,则三种元素原子序数的大小顺序为()
| A.X>Y>Z | B.Y>X>Z | C.X>Z>Y | D.Z>X>Y |