根据下列实验现象,所得结论正确的是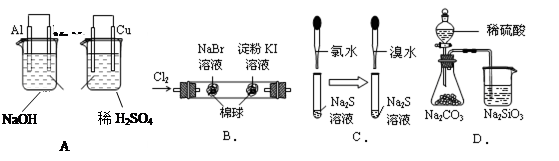

| 实验 |
实验现象 |
结论 |
| A. |
左烧杯中镁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Mg>Cu |
| B. |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
| C. |
左边溶液产生黄色沉淀,右边溶液产生黄色沉淀 |
氧化性:Cl2>Br2>S |
| D. |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:S>C>Si |
短周期元素X、Y、Z在元素周期表中的位置如下图所示,下列说法正确的是()
| X |
||
| Y |
||
| Z |
A.X、Y、Z三种元素中,X的非金属性最强
B.原子半径的大小顺序:Z>Y
C.Y的最高正化合价为+7
D.Y的氢化物的稳定性比Z的弱
下列叙述正确的是()
| A.越难失电子的元素得电子能力一定越强 |
| B.溶于水可以导电的化合物一定是离子化合物 |
| C.第三周期元素的最高正化合价等于它所处的主族序数 |
| D.离子化合物中可以含有共价键,共价化合物可以含有离子键 |
下列关于热化学方程式 H2(g)+
H2(g)+ I2(g)=HI(g) △H=-4.5 kJ•mol-1的叙述正确的是( )
I2(g)=HI(g) △H=-4.5 kJ•mol-1的叙述正确的是( )
| A.1mol H2和1mol I2完全反应放出4.5kJ热量 |
| B.1个氢分子和1个碘分子完全反应放出9kJ热量 |
| C.1mol H2和1mol I2完全反应生成气态HI放出9kJ热量 |
| D.0.5mol H2和0.5mol I2完全反应需要吸收4.5kJ热量 |
下列关于化学键的说法正确的是()
| A.单质分子中一定含有共价键 |
| B.由非金属元素组成的化合物不一定是共价化合物 |
| C.化学键是相邻的分子之间强烈的相互作用 |
| D.阴、阳离子通过静电吸引所形成的化学键,叫离子键 |
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图所示。已知断裂1mol N—N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,判断下列说法正确的是()
| A.N4属于一种新型的化合物 | B.N4晶体熔点高,硬度大 |
| C.相同质量的N4能量高于N2 | D.1mol N4转变成N2将吸收882 kJ热量 |