(1)写出下列反应的离子方程:
①在NaOH溶液通入少量二氧化碳: 。
②向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性: 。
(2)软锰矿(MnO2)和过量的固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl,写出软锰矿制备K2MnO4的化学方程式,并标出电子转移的方向和数目:
为除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)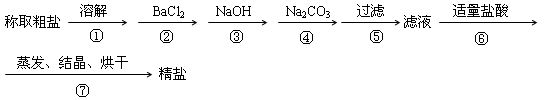
(1)判断BaCl2已过量的方法是
(2)在第⑥步中,写出所有反应的化学方程式
(1)同温同压下,两种气体A和B的体积之比为2:1,质量之比为8:5,则A与B的密度之比为,摩尔质量之比为。
(2)在标准状况下a. 6.72L CH4气体 b.3.01×1023个HCl气体分子 c.13.6g H2S气体 d.0.2molNH3,下列对这四种气体的关系从大到小的排列是(用上述序号表示)
①四种气体的物质的量,
②标准状况下四种气体的体积,
③四种气体的质量。
(6分)物质的量相等的 CO 和 CO2中,分子个数之比为 ____;原子个数之比为 _________;氧原子个数比为。
(14分) (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示________________,K值大小与温度的关系是:温度升高,K值__________(填一定增大、一定减小、或可能增大也可能减小)。
(2)已知反应Cl2+H2O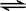 HCl+HClO,写出该反应化学平衡常数的表达式
HCl+HClO,写出该反应化学平衡常数的表达式
(3)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)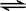 CO2(g)+H2 (g) ΔH=-QkJ/mol (Q>0)
CO2(g)+H2 (g) ΔH=-QkJ/mol (Q>0)
CO和H2O浓度变化如下图,则0~4 min的平均反应速率v(CO)=______ mol/(L·min)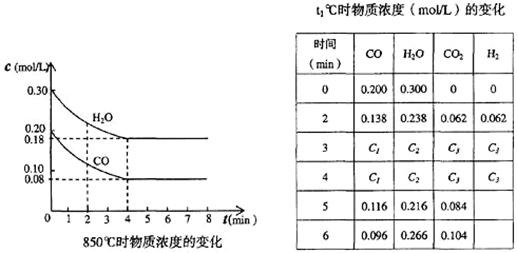
(4)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3 min~4 min之间反应处于_________状态;C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4 min~5 min问,平衡向逆方向移动,可能的原因是_______,表中5 min~6 min之间数值发生变化,可能的原因是_______。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
现有T1℃的密闭容器中存在如下反应:2SO2 (g) + O2(g)  2SO3(g) △H<0。已知c(SO2)始=0.4mol/L,c(O2)始=1mol/L经测定该反应在该温度下的平衡常数K≈19,试判断:
2SO3(g) △H<0。已知c(SO2)始=0.4mol/L,c(O2)始=1mol/L经测定该反应在该温度下的平衡常数K≈19,试判断:
(1)当SO2转化率为50%时,该反应是否达到平衡状态,理由是;若未达到,反应向进行。(填“正反应”或“逆反应”)
(2)已知T2>T1,则该反应T2℃下的平衡常数________19。(填“>”“<”或“=”)
(3)达平衡状态时, SO2的转化率α应为(列出与α有关的计算公式即可)