下表是A、B两种有机物的有关信息: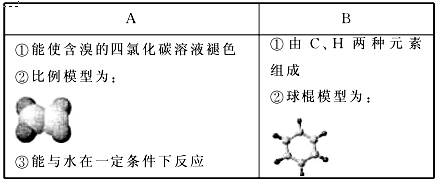
 根据表中信息回答下列问题:
根据表中信息回答下列问题:
(1)A与含溴的四氯化碳溶液反应的生成物的名称为________________;
写出在一定条件下,A与水反应的化学反应方程式___________。
(2)A的同系物用通式Cn Hm表示,B的同系物用通式Cx Hy表示,当A、B同系物分别出现同分异构体时,碳原子数最小值n =________,x =________。
(3)B具有的性质是______________(填序号)。
①无色无味液体;②有毒;③不溶于水;④密度比水大; ⑤与酸性KMnO4溶液和溴水反应使之褪色;⑥任何条件下不与氢气反应;⑦使溴水颜色变浅或褪色
(14分)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上常用CO和H2反应生产CH3OH,并开发出甲醇燃料电池。
(1)已知:CO(g)+1/2O2(g)=CO2(g)△H=-283.0 kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1453.0 kJ·mol-1
则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为。
(2)工业上常利用反应CO(g)+2H2(g) CH3OH(g) △H<0合成甲醇,在230℃~270℃最为有利。为研究合成气最合适的起始组成比,分别在230℃、250℃和270℃进行实验,结果如图。
CH3OH(g) △H<0合成甲醇,在230℃~270℃最为有利。为研究合成气最合适的起始组成比,分别在230℃、250℃和270℃进行实验,结果如图。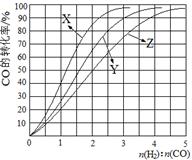
230℃的实验结果所对应的曲线是(填字母);该温度下工业生产适宜采用的合成气组成n(H2):n(CO) 的比值范围是(填字母) 。
A.1~1.5 B.2.5~3 C.3.5~4.5
(3)制甲醇所需要的氢气,可用下列反应制取:H2O(g)+CO(g) H2(g)+CO2(g) △H<0,某温度下该反应的平衡常数K=1。试回答下列问题:
H2(g)+CO2(g) △H<0,某温度下该反应的平衡常数K=1。试回答下列问题:
①该温度下,若起始时c(CO)="1" mol·L-1,c(H2O)="2" mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应v(正)v(逆)(填“>”、“<”或“=”)。
②若降低温度,该反应的K值将(填“增大”、“减小”或“不变”)。
(4)某实验小组设计了如图所示的甲醇燃料电池装置。
①该电池工作时,OH-向极移动(填“a”或“b”)。
②工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为。
工业上生产高氯酸(沸点:90oC)时还生产了亚氯酸钠,其工艺流程如下:
(1)冷却过滤的目的是降低NaHSO4的,并分离出NaHSO4晶体。
(2)反应器2中发生反应的离子方程式为,SO2的作用是作剂。
(3)上述工业生产高氯酸的化学反应为:3NaClO3+3H2SO4(浓)=3NaHSO4+HClO4+2ClO2+H2O,氧化产物与还原产物的物质的量之比为。
(4)可以通过蒸馏滤液的方法得到高氯酸的原因可能是高氯酸的沸点比较(填“高”或“低”),容易从溶液中逸出,循环使用的物质是。
(共12分)某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金属屑制取新型高效水处理剂Na2FeO4(高铁酸钠)等产品,过程如下:
I. 向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
II. 向I所得固体中加入过量稀H2SO4,充分反应后过滤;
III. 向II所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
IV. ……
(1)步骤I中发生反应的化学方程式为、。
(2)步骤II所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因。
(3)步骤III获得CuSO4溶液的离子方程式为。
(4)步骤II所得滤液经进一步处理可制得Na2FeO4,流程如下:
写出由Fe(OH)3制取Na2FeO4的化学方程式___________。
化学用语是化学学科的特色语言,化学用语可以准确表述化学现象、变化以及本质,请按要求完成以下两个问题。
(1)配平酸性高锰酸钾溶液与过氧化氢溶液反应的离子方程式:
H2O2+ MnO4-+=Mn2++O2↑+
(2)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:____________________、_______________________。
简要回答下列问题(并写出问题1、2、4的方程式)
(1)镁燃烧时不能用二氧化碳来扑灭,其原因是。
(2)为什么不能用铜制容器盛氯化铁溶液?。
(3)当人误食重金属盐时,可以喝大量牛奶、蛋清或生豆浆解毒。重金属盐使人中毒的原因是:。
(4)冬季,渔民常在放干水的池塘里遍撒一些漂白粉,其目的是。