胶体区别于其它分散系最本质的特征是( )
| A.外观澄清、透明 | B.胶体微粒粒度在1~100nm之间 |
| C.丁达尔现象 | D.分散质粒子能透过半透膜 |
银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是()
| A.锌为正极,Ag2O为负极; | B.锌 为阳极,Ag2O为阴极; 为阳极,Ag2O为阴极; |
| C.原电池工作时,负极区PH减小; | D.原电池工作时,负极区PH增大; |
在一定温度下,反应A2(气)+B2(气)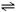 2AB(气)达到平衡的标志是 ( )
2AB(气)达到平衡的标志是 ( )
A.单位时间内生成nmolA2同时生成nmol的AB |
| B.容器内总压强不随时间而变化 |
| C.单位时间内生成2nmolAB,同时生成nmol的B2 |
D.单位时间 生成nmolA2,同时生成nmol的B2 生成nmolA2,同时生成nmol的B2 |
已知:CH4(g)+2O2(g)==CO2(g)+2H2O(1)△H="―Q1" KJ/mol 2H2(g)+O2(g)==2H2O(g) △H=―Q2 KJ/mol 2H2(g)+O2(g)==2H2O(1) △H = ―Q3KJ/mol常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况),经完全燃烧后恢复至常温,则放出的热量为多少KJ()
| A.0.4Q1+0.1Q2 | B.0.4Q1+0.05Q2 | C.0.4Q1+0.1Q3 | D.0.4Q1+0.05Q3 |
碳酸铵((NH4)2CO3)在室温下就能自发地分解产生氨气,对其说法中正确的是( )
)
| A.其分解是因为生成了易挥发的气体,使体系的熵增大 | B.其分解是因为外界给予了能量 |
| C.其分解是吸热反应,据能量判据不能自发分解 | D.碳酸盐都不稳定,都能自发分解 |
下列关于铜电极的叙述,正确的是()
| A.铜锌原电池中铜是正极 |
| B.用电解法精炼粗铜时铜作阳极 |
| C.在镀件上电镀铜时可用金属铜作阳极 |
| D.电解稀硫酸制H2、O2时铜作阳极 |