今有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
| A.K+一定存在 | B.100mL溶液中含0.01molCO32- |
| C.Ba2+一定不存在,Mg2+可能存在 | D.不可能存在Cl- |
C、N、S都是重要的非金属元素。下列说法正确的是
A.三者对应的氧化物均为酸性氧化物
B.实验室可用NaOH溶液处理SO2、NO2
C.CO2、NO2、SO2都能与H2O反应,其反应原理相同
D.三者的单质直接与氧气反应都能生成两种氧化物
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
| A.X、Y的简单离子半径:r(X2-)<r(Y+) |
| B.M的气态氢化物比N的气态氢化物稳定 |
| C.M与X形成的化合物对应的水化物一定是强酸 |
| D.Y2X和Y2X2中阴、阳离子的个数比相同,但化学键类型不同 |
符合下图的化学反应是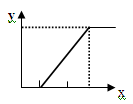
| x轴 |
y轴 |
||
| A |
向氯化铝溶液中加入氢氧化钠溶液 |
氢氧化钠的物质的量 |
生成沉淀的质量 |
| B |
向碳酸钠溶液中加入稀盐酸 |
盐酸的体积 |
产生气体的体积 |
| C |
向溴化亚铁溶液中通入氯气 |
氯气的体积 |
生成Br2的物质的量 |
| D |
向氢氧化钙溶液中通入二氧化碳 |
二氧化碳的体积 |
生成碳酸氢钙的质量 |
据最新报道,科学家发现了如下反应:O2+PtF6 = O2(PtF6),已知O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列叙述正确的是
| A.在此反应中,O2是氧化剂,PtF6是还原剂 |
| B.反应中每生成1molO2(PtF6)转移1mol电子 |
| C.O2(PtF6)中氧元素的化合价是+1价 |
| D.O2(PtF6)中仅存在离子键不存在共价键 |
酸性溶液中,Fe2+会被空气缓慢氧化为Fe3+。不同条件下,一定浓度的Fe2+的氧化率随时间变化关系如图所示。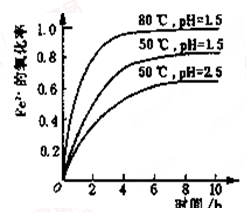
下列有关说法正确的是
| A.该氧化过程的离子方程式为:Fe2++O2+4H+=Fe3++2H2O |
| B.其他条件相同时,80℃时Fe2+的氧化率比50℃的大 |
| C.Fe2+的氧化率仅与溶液的pH和温度有关 |
| D.pH=1.5时Fe2+的氧化率一定比pH=2.5的大 |