下列离子方程式书写正确的是 ( )
| A.Na2HPO4溶于水:Na2HPO4=2Na++H++PO43- |
| B.NaHCO3溶液的水解离子方程式:HCO3- + H2O = H3O+ + CO32- |
C.HF溶 于少量水中: 2HF=H++HF2一 于少量水中: 2HF=H++HF2一 |
| D.(NH4)2 SO4溶于水:(NH4)2 SO4=2 NH4++SO42一 |
能正确表示下列反应的离子方程式为
| A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C.NaClO和NaOH的混合溶液中通入少量的SO2:ClO-+H2O+SO2=Cl-+SO42-+2H+ |
| D.大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
下列关于离子的检验方法一定正确的是
| A.向某溶液中滴加BaCl2溶液,若有白色沉淀,则滴加足量稀HNO3,若有沉淀不溶解,则说明原溶液中一定含Ag+ |
| B.向某溶液中滴加浓NaOH溶液,产生的气体使湿润的红色石蕊试纸变蓝色,说明原溶液中含有NH4+ |
| C.向某溶液中滴加足量稀HCl,产生气体使澄清石灰水变浑浊,则说明原溶液中一定含CO32- |
| D.用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色未见紫色,则说明原溶液中不含K+ |
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象.为确定该溶液的组成,还需检验的离子是
| A.SO42- | B.Na+ | C.Ba2+ | D.NH4+ |
下列实验现象预测正确的是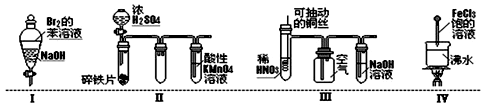
| A.实验Ⅰ:振荡后静置,溶液不再分层,且保持无色透明 |
| B.实验Ⅱ:铁片最终完全溶解,且高锰酸钾溶液变无色 |
| C.实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终无明显变化 |
| D.实验Ⅳ:当溶液至红褐色,停止加热,让光束通过体系时可产生丁达尔现象 |
除去下列物质中所含的杂质,选用的试剂正确的是
| 选项 |
物质(杂质) |
试剂 |
| A |
食盐(细沙) |
NaOH溶液 |
| B |
CO(NH3) |
浓H2SO4 |
| C |
CO2(SO2) |
Na2CO3溶液 |
| D |
NaHCO3溶液(Na2CO3) |
Ca(OH)2溶液 |