某可逆反应的平衡常数表达式 ,恒容时,温度升高H2浓度减小。试回答
,恒容时,温度升高H2浓度减小。试回答 下列问题:
下列问题:
(1)该反应的化学方程式为:  。
。
(2)温度升高,该反应的K值______________(填“增大”“减小”或“不变”),化学平衡移动达到新的平衡后,CO2和CO体积比___________(填“增大”“减小”或“不变”)。
(3)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生反应,CO和H2O浓度变化如下图。则 0—4min的平均反应速率v(CO)=___________ mol/(L·min),850℃的化学平衡 常数的值K=
常数的值K= 
(4)850℃时,在相同容器中发生反应CO2+ H2 CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、 二氧化碳0.08 mol/L、氢气 0.08
CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、 二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时v(正) v(逆)(“大于”“ 小于”或“等于”)
mol/L,此时v(正) v(逆)(“大于”“ 小于”或“等于”)
(10)氧族元素的各种性质可归纳整理如下(部分):
| 元素 性质 |
8O |
16S |
Se |
52Te |
| 单质沸点(℃) |
-183 |
444.6 |
685 |
1390 |
| 主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
|
| 原子半径(nm) |
0.074 |
0.102 |
0.116 |
0.143 |
| 单质与H2反应 |
点燃易化合 |
加热化合 |
加热难化合 |
不能直接化合 |
回答下列问题:
(1)氧离子的结构示意图为,硫离子的电子式为。
(2)碲的主要化合价可能有。
(3)氧元素比硫无素非金属性(填强和弱)。请用化学方程式证明该结论:
(4)H2O2可以作脱氯剂,用于消除水中的Cl2,写出该反应的化学方程式:
(10)已知A、B、C、D为原子序数依次增大的短周期元素,其中A、D同主族.A元素的单质是密度最小的气体,B元素原子的最外层电子数是次外层电子数的2倍,且其最外层电子数比C元素原子的最外层电子数少2。
试回答下列问题:
(1)写出B的元素符号:。
(2)C在元素周期表中的位置为。
(3)写出BA4的电子式:
(4)用电子式表示离子化合物D2C的形成过程。
(5)写出D2C2与A2C反应的化学方程式:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同。回答下列问题: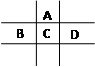
(1)①A与E形成的化合物的化学式是。
②B的最高价氧化物化学式为。
③C的元素名称为。
(2)D的单质与水反应的方程式为:。
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是,有关反应的离子方程式为:
,。
A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)①A原子的结构示意图为,
②B原子的电子式为,
③D的氢化物的电子式为,
④E的最高价氧化物的化学式为。
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A、B最高价氧化物对应水化物相互反应的化学方程式:
(4)比较C、D的最高价氧化物的水化物的酸性:(用化学式表示):
下表是周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
族 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
||
| 1 |
A |
|||||||||
| 2 |
D |
E |
G |
I |
||||||
| 3 |
B |
C |
F |
H |
(1)表中元素,化学性质最不活泼的是 ,只有负价而无正价的是 ,氧化性最强的单质是 ,还原性最强的单质是 ;
(2)最高价氧化物的水化物碱性最强的碱是 ,酸性最强的酸是 ,呈两性的物质是 ;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的 ;
(4)在B、C、D、E、F、G、H中,原子半径最大的是 ,最小的是 。