下列推断正确的是
A. 是酸性氧化物,能与NaOH溶液反应 是酸性氧化物,能与NaOH溶液反应 |
B. 组成元素相同,与 组成元素相同,与 反应产物 反应产物 也相同 也相同 |
C.CO、NO、 都是大气污染气体,在空气中都能稳定存在 都是大气污染气体,在空气中都能稳定存在 |
| D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
已知短周期元素的离子aA2+、bB+、cC3–、dD–都具有相同的电子层结构,则下列叙述正确的是()
A.原子半径:r(A)>r(B)>r(D)>r(C) B.原子序数:b>a>c>d
C.离子半径:r(C3–)>r(D–)>r(B+)>r(A2+)D.单质的还原性:A>B>D>C
短周期元素X、Y可以形成化合物XY2,下列有关叙述不正确的是( )
| A.若XY2是共价化合物,则X与Y的原子序数可能相差1 |
| B.若XY2是离子化合物,则X与Y的原子序数可能相差8 |
| C.若X与Y的原子序数相差5,则离子化合物XY2中X的离子半径比Y离子半径小 |
| D.若X与Y的原子序数相差6,则共价化合物XY2可溶于强碱溶液 |
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是( )
A.元素B、E组成的化合物常温下呈气态
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应
C. C、D、E的半径:C>D>E
D.化合物AE与CE具有相同类型的化学键
某元素的一种同位素X原子的质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX分子中含质子的物质的量是( )
A.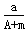 (A+N+m)mol (A+N+m)mol |
B.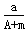 (A-N+m)mol (A-N+m)mol |
C.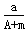 ( A-N)mol ( A-N)mol |
D.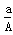 (A-N)mol (A-N)mol |
在一定条件下,RO3-与R-可发生反应:RO3-+5R-+6H+== 3R2+3H2O,下列关于R元素的叙述中,正确的是( )
| A.元素R位于周期表中第ⅤA族 |
| B.RO3-中的R只能被还原 |
| C.R2在常温常压下一定是气体 |
| D.若1 mol RO3-参与该反应,则转移的电子的物质的量为5 mol |