若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是
| A.生成了一种强酸弱碱盐 | B.弱酸溶液和强碱溶液反应 |
| C.强酸溶液和弱碱溶液反应 | D.一元强酸溶液和一元强碱溶液反应 |
只用一种试剂就能鉴别AgNO3溶液、乙醇溶液、苯酚溶液、烧碱溶液、硫氰化钾溶液。该试剂是( )
| A.溴水 | B.盐酸 |
| C.石蕊试液 | D.氯化铁溶液 |
漆酚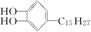 是生漆的主要成分,黄色,能溶于有机溶剂中。漆酚不具有的化学性质有( )
是生漆的主要成分,黄色,能溶于有机溶剂中。漆酚不具有的化学性质有( )
| A.可以燃烧,当氧气充足时,产物为CO2和H2O |
| B.与FeCl3溶液发生显色反应 |
| C.能与NaOH溶液反应,也能与Na2CO3溶液反应产生气泡 |
| D.它能与浓溴水发生取代反应和加成反应,且1 mol漆酚最多消耗5 mol Br2 |
关于实验室制取乙烯的实验,下列说法正确的是( )
| A.反应物是乙醇和过量的3 mol/L硫酸的混合液 |
| B.温度计插入反应溶液液面以下,以便控制温度在140 ℃ |
| C.反应容器(烧瓶)中应加入少许碎瓷片 |
| D.反应完毕后先熄灭酒精灯火焰再从水中取出导管 |
下列乙醇的化学性质中不是由羟基所决定的是( )
| A.在足量O2中完全燃烧生成CO2和H2O |
| B.跟活泼金属Na等发生反应 |
| C.当Ag或Cu存在时跟O2发生反应生成CH3CHO和H2O |
| D.在浓硫酸存在条件下加热到170 ℃生成CH2CH2 |
下列叙述正确的是( )
| A.酚醛树脂是通过苯酚与甲醛经加聚反应制得的 |
| B.将苯酚晶体放入少量水中,加热时全部溶解,冷却到50 ℃形成悬浊液 |
| C.苯酚的酸性很弱,不能使酚酞指示剂变色,但可以和碳酸氢钠反应放出CO2 |
| D.向苯酚的水溶液中滴加FeCl3溶液,溶液变紫色 |