12mL浓度为0.1mol·L-1Na2SO4溶液,恰好与40mL浓度为0.01 mol·L-1K2Cr2O7溶液完全反应,则元素Cr在被还原的产物中得化合价是
| A.0 | B.+2 | C. +3 | D.+6 |
高铁酸钠(Na2FeO4)的氧化性强于高锰酸钾和臭氧,是一种高效多功能净水混凝剂。下面关于高铁酸钠净水作用的叙述不正确的是
A Na2FeO4在净水过程中能转变成氢氧化铁
B Na2FeO4能杀菌消毒
C Na2FeO4能除去水中的硫化氢等还原性气体杂质
D Na2FeO4能吸附水中的颜色和固体颗粒
下列制备设计错误的是
| A.以苯为原料制水杨酸(邻羟基苯甲酸),应向苯环上先引入酚羟基 |
| B.制备表面活性剂对十二烷基苯磺酸钠,可向苯环上先引入磺酸基(-SO3H) |
| C.制备十二烷基苯可以采用1-十二烯在一定条件下与苯加成 |
| D.采用对MgCl2·6H2O在氯化氢气流中加热脱水制无水MgCl2 |
在PVC、PE、PP、ABS中,通过共聚而得到的类似“合金化”的高分子材料为
A. PVCB. PEC. PPD. ABS
化学与生产、生活、社会密切相关。下列有关说法中,错误的是
| A.利用可降解的“玉米塑料”替代一次性饭盒,可防止产生白色污染 |
| B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
| C.食品工业利用液态二氧化碳代替有机溶剂,能避免有机溶剂污染食品 |
| D.自来水用臭氧消毒是利用臭氧的强漂白性 |
. 已知:还原性 ,氧化性
,氧化性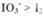 。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法正确的是
。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法正确的是
| A.反应过程中的氧化产物均为SO3 |
| B.a点时剩余NaIISO3的物质的量为1.2 mol |
| C.b点时的还原产物可能是KI或NaI |
| D.当溶液中r与I2的物质的量之比为1:1时,加入的KIO3为1.1 mol |