通过下列实验比较① ② CH3CH2OH ③ H-OH ④
② CH3CH2OH ③ H-OH ④
⑤ 五种物质中羟基上氢原子的活泼性顺序。在下表中填写实验现象及实验结论。
五种物质中羟基上氢原子的活泼性顺序。在下表中填写实验现象及实验结论。
| 编号 |
实验操作 |
实验现象 |
实验结论 |
| 1 |
分别取上述五种物质的少量溶液或液体于试管中,各滴入几滴石蕊试液 |
|
|
| 2 |
分别取适量①、⑤的水溶液,各加入少量NaHCO3固体 |
|
|
| 3 |
分别取少量②、③、④,各加入适量NaOH溶液,再通入足量CO2 |
|
|
| 4 |
分别取少量②、③的液体,各加入一小粒金属钠 |
|
|
结论:上述五种物质中的羟基上氢原子活泼性顺序为 (填序号)
金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)CaO。
(1)Ca原子结构示意图 。
(2)Ca与最活跃的非金属元素A形成化合物D,D的沸点比A与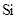 形成的化合物E的沸点 (填高或低),用电子式表示D的形成过程 。
形成的化合物E的沸点 (填高或低),用电子式表示D的形成过程 。
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n。则M位于元素周期表中的位置是: 。
(4)取1.6g钙线试样,与水充分反应,生成224ml H2(标准状况),再向溶液中通入适量的CO2,最多能得到CaCO3 g.
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的轨道表示式为__________________;
(2)五种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
(3)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的分子空间构型为____________,A的电子式为____________,B的结构式为____________。
(4)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层。该族2-- 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。]
a.+99.7 kJ·mol-1 b.+29.7 kJ·mol-1
c.-20.6 kJ·mol-1 d.-241.8 kJ·mol-1
(5)工业上常用电解M2L3的方法来制取M单质。当制得54克M单质时,转移电子的物质的量是_________ mol。
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z |
Z和Y同周期,Z的电负性大于Y |
| W |
W的一种核素的质量数为63,中子数为34 |
(1)Y的元素符号是 。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子核外电子排布式是 。
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。此反应的化学方程式是 。
(5)请设计一个实验方案,比较Y、Z单质氧化性的强弱:________________________。
现用Na2CO3固体配制500mL 0.200 mol·L-1的Na2CO3溶液。可供选择的仪器有:①玻璃棒;②烧瓶;③烧杯;④胶头滴管;⑤漏斗;⑥天平;⑦药匙
请回答下列问题:
(1)上述仪器中,在配制Na2CO3溶液时不需要使用的有 (填代号),还缺少的仪器是 (填仪器名称)。
(2)经计算,需Na2CO3固体质量为 。
(3)将所配制的Na2CO3溶液进行测定,发现浓度小于0.200 mol·L-1。请你分析配制过程中可能引起误差偏小的原因 。
A.Na2CO3固体中含结晶水
B.转移时没有洗涤烧杯和玻璃棒
C.配制时容量瓶没有干燥
NaCl是一种化工原料,可以生产一系列物质(见下图)。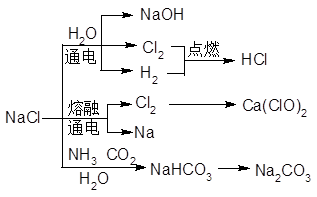
(1)25℃,NaHCO3在水中的溶解度比Na2CO3的_____(填“大”、“小”或“不能确定”)
(2)已知氯化钠在25℃的溶解度为36g,则该温度下饱和氯化钠的质量分数为______(计算结果保留一位小数)。
(3)碳酸氢钠受热分解的化学方程式是_______
(4)用氯气生产氯化氢的化学方程式是________
(5)食盐水通电后发生反应的离子方程式是_______