在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应:A(S)+3B(g)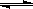 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A.混合气体的压强不随时间变化 B. B的生成速率和D的消耗速率为3︰1
C.混合气体的密度不随时间变化 D. B、C、D的分子 数之比为3︰2︰1
数之比为3︰2︰1
下列仪器:①量筒②表面皿③烧杯④试管⑤容量瓶⑥蒸发皿⑦坩埚⑧烧瓶,能直接用酒精灯加热的是
| A.②③④⑥⑦⑧ | B.③④⑥⑦⑧ | C.④⑥⑦ | D.④⑦⑧ |
下列叙述正确的是
| A.由X变为X2-的反应是氧化反应 |
| B.某反应中的氧化剂也可能有还原性 |
| C.失去电子数多的还原剂,还原性一定强 |
| D.有单质参加或生成的反应一定是氧化还原反应 |
在配制一定物质的量浓度的NaCl溶液时,下列操作会造成所配溶液浓度偏高的是
| A.在用托盘天平称量所需NaCl的质量时,左盘放砝码右盘放NaCl |
| B.定容时俯视刻度线 |
| C.转移时,把烧杯和玻璃棒用蒸馏水洗涤并把洗涤液也转移至容量瓶 |
| D.容量瓶中有少量水,转移溶液前将容量瓶烘干 |
今有0.1mol/L NaCl溶液300mL,0.1mol/L MgCl2溶液200mL,0.1mol/L AlCl3溶液100mL,这三种溶液中Cl-物质的量浓度之比是
| A.3∶4∶3 | B.3∶2∶3 | C.1∶2∶3 | D.1∶1∶1 |
只能表示一个化学反应的离子方程式是
| A.H+ + OH- = H2O |
| B.CO32-+ 2H+ = H2O +CO2 ↑ |
| C.Mg(OH)2+2H+=Mg2++2H2O |
| D.Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓ |