对于可逆反应A(g)+2B(g)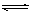 2C(g)(正反应吸热),下列图象中正确的是( )
2C(g)(正反应吸热),下列图象中正确的是( )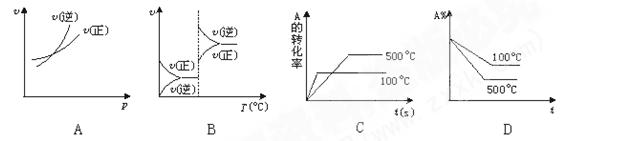
将淀粉浆和淀粉酶的混合物放入半透膜袋中,扎好后浸入流动的温水中,经过足够的时间后,取出袋内的液体,分别与①碘水' ②新制Cu(OH)2悬浊液(加热)' ③浓硝酸(微热)作用,其现象依次是
| A.显蓝色;无红色沉淀;显黄色 |
| B.不显蓝色;无红色沉淀;显黄色 |
| C.显蓝色;有红色沉淀;不显黄色 |
| D.不显蓝色;有红色沉淀;不显黄色 |
化学与社会、生产、生活紧切相关。下列说法正确的是
| A.棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 |
| B.石油干馏可得到石油气、汽油、煤油、柴油等 |
| C.从海水中提取物质都必须通过化学反应才能实现 |
| D.纯碱可用于生产普通玻璃,日常生活中也可用纯碱溶液来除去物品表面的油污 |
下列化合物,既能发生水解反应又能发生银镜反应的是
| A.甲酸丙酯 | B.乙酸乙酯 | C.2-羟基丁醛 | D.丁酸 |
为验证淀粉水解可生成还原性糖进行了下列实验,该实验中操作步骤的排列顺序正确的是
①取少量淀粉加水制成悬浊液②加热煮沸
③加入新制的Cu(OH)2悬浊液 ④加几滴稀硫酸
⑤再加热直至沸腾 ⑥加入碱液,中和直至溶液呈碱性
| A.①②④⑤③⑥ | B.①④②③⑤⑥ |
| C.①④②⑥③⑤ | D.①⑤③④⑥② |
某同学为了检验纤维素的水解产物是否为葡萄糖,他将纤维素与70%的硫酸共热后加入新制Cu(OH)2悬浊液并加热煮沸,无红色沉淀生成,以下解释正确的是
| A.纤维素水解产物中无葡萄糖 |
| B.使用的硫酸过浓只发生了脱水反应 |
| C.由于水解后混合液中含有H2SO4,所以见不到红色沉淀 |
| D.加热时间不够长,所以见不到砖红色沉淀 |