已知NH3和HCl都能用来作喷泉实验的气体,若在同温同压下用等体积
烧瓶各收集满NH3和HCl气体,实验后二个烧瓶内溶液的关系是
(两烧瓶内充满溶液且不考虑溶质的扩散) 
| A.溶质的物质的量浓度相同、溶质的质量分数不同 |
| B.溶质的质量分数相同,溶质的物质的量浓度不同 |
| C.溶质的物质的量浓度和溶质的质量分数都不同 |
| D.溶质的物质的量浓度和溶质的质量分数都相同 |
卤代烃能发生下列反应:2CH3CH2Br + 2Na → CH3CH2CH2CH3 + 2NaBr。
下列有机物中,可合成环烷烃的是
A.CH3CH2CH2Br |
B.CH3 CH2CHBr2 |
| C.CH2BrCH2CH2Br | D.CH3CHBrCH2CH2Br |
某有机物的化学式为C5H10O,它能发生银镜反应和加成反应。若将它与H2加成,所得产物结构简式可能是
| A.(CH3)3CCH2OH | B.(CH3CH2)2CHOH |
| C.CH3(CH2)3CH2OH | D.CH3CH2C(CH3)2OH |
下列各组中的两种有机物,其最简式相同但既不是同系物,又不是同分异构体的是
| A.苯苯乙烯 | B.甲醛乙酸 | C.对甲基苯酚苯甲醇 | D.甲酸乙醛 |
下列有机物的名称中不正确的是
| A.3—乙基戊烷 | B.2,3—二甲基戊烷 |
| C.2,2—二甲基—2—乙炔 | D.2—甲基—4—乙基庚烷 |
含有一个叁键的炔烃,氢化后产物的结构简式为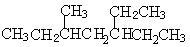 。此炔
。此炔 烃可能具有的结构式有
烃可能具有的结构式有
| A.1种 | B.2种 | C.3种 | D. 4种 4种 |