目前,人们正在研究开发一种高能电池---钠硫电池,它是以熔融的钠和硫为两极,以Na+导电的β′—Al2O3陶瓷作固体电解质,反应式如下:Na2Sx 2Na+xS,以下说法正确的是 ( )
2Na+xS,以下说法正确的是 ( )
| A.放电时,Na 作正极,S极发生还原反应 |
| B.充电时钠极与外电源的正极相连 |
| C.当用该电池电解AgNO3溶液时,阳极上产生标况下气体11.2L时,消耗钠2.3g |
| D.充电时,阳极发生的反应为:Sx2--2e-=xS |
2.下列化学用语错误的是
A.羟基电子式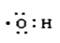 |
| B.乙烯的结构简式 CH2CH2 |
| C.乙酸的实验式CH2O |
D.3,3-二甲基-1-戊烯的键线式: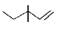 |
1.下列关于“生活中的化学”的叙述不正确的是
| A.棉花和蚕丝的主要成分都是纤维素 |
| B.误食重金属盐,可立即喝牛奶或鸡蛋清解毒 |
| C.食用植物油的主要成分是高级不饱和脂肪酸甘油酯 |
| D.新居室内装饰材料中缓慢释放出甲醛、甲苯等有机物会污染室内空气 |
14.1905年德国化学家哈伯发明了合成氨的方法。他因此获得了1918年度诺贝尔化学奖。哈伯法合成氨需要在20—50 MPa的高压和500 ℃的高温下,用铁作催化剂,且氨转化率10%—15%。2005年6月27日美国化学会刊报道,美国俄勒冈大学的化学家使用了一种名为transFe(DMeOPrPE)2Cl2的铁化合物。用transFe(DMeOPrPE)2Cl2作催化剂,在常温常压下合成出氨,反应可表示为N2+3H2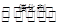 2NH3,有关说法正确的是
2NH3,有关说法正确的是
| A.不同的催化剂对化学反应速率影响均相同 |
| B.新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展远景 |
| C.新法合成能在常温下进行是因为不需要断裂化学键 |
| D.哈伯法合成氨是吸热反应,新法合成氨是放热反应 |
30、2N2O5(g)=4NO2(g)+O2(g) △H=+56.8kJ/mol自发进行的原因是
| A.是吸热反应; |
| B.是放热反应; |
| C.是熵减少的反应; |
| D.熵增大效应大于能量效应。 |
29.下列说法正确的是
| A.某反应低温条件下能自发进行,那么高温条件也一定能自发进行 |
| B.某反应高温条件下不能自发进行,那么低温条件也不能自发进行 |
| C.反应方向是由焓变和熵变共同决定的,与反应温度无关 |
| D.温度有可能对反应的方向起决定性的作用 |