将洁净的金属片A、B、C、D分别放置在浸有某种盐溶液的滤纸上面并压紧(如下图所示)。在每次实验时,记录电压指针的移动方向和电压表的读数如下: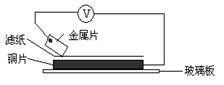
已知,构成两电极的金属其金属活泼性相差越大,电压表的读数越大。
金属 电子流动方向 电压/V
A A→Cu +0.78
B Cu→B -0.15
C C→Cu +1.35
D D→Cu +0.30
请依表中数据判断,下列有关说法正确的是( )
①在四种金属中C的还原最强 ②金属B能从硫酸铜溶液中置换出铜
③A、D若形成原电池时,A为正极④A、B形成合金时,将该合金露置在空气中,A先被腐蚀
A①② B②③ C①③ D①④
下列各组离子,一定能在指定环境中大量共存的是
| A.在含有大量I-离子的溶液中:Cl¯、Fe3+、Al3+、Cu2+ |
| B.滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、NO3-能够大量共存 |
| C.在由水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、Cl¯、Br¯ |
| D.在加入Al能放出大量H2的溶液中:NH4+、SO42¯、C1¯、HCO3¯ |
有关下列有机物的说法正确的是
| A.它是一种二肽 | B.完全水解可得三种氨基酸 |
| C.它只能与氢氧化钠溶液反应 | D.一个分子中含有三种含氧官能团 |
区别硫酸铜溶液和氢氧化铁胶体最简单的方法是
| A.观察溶液颜色 | B.丁达尔效应 | C.过滤 | D.加热 |
Fe(OH)3胶体稳定存在的主要原因是
| A.胶粒做布朗运动 | B.胶粒带正电荷 |
| C.胶粒直径小于1nm | D.胶粒不能通过半透膜 |
下列叙述不正确的是
| A.光照氯水有气泡逸出,该气体是Cl2 |
| B.工业上可用碳在高温下还原二氧化硅制取硅 |
| C.工业上可用氯气和石灰乳为原料制造漂白粉 |
| D.将盛有氢氧化铁胶体的烧杯置于暗处,用一束光照射,从垂直于光线的方向可以观察到一条光亮的通路 |