铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。 (1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O 3(s) + 3CO(g)
3(s) + 3CO(g) 2Fe(s) + 3CO2(g)
2Fe(s) + 3CO2(g)
 ①该反应的平衡常数表达式为:K=
①该反应的平衡常数表达式为:K=  ②该温度下,在2L盛有
②该温度下,在2L盛有 粉末的密闭容器中通入CO气体,10min后,生成了单
粉末的密闭容器中通入CO气体,10min后,生成了单 质铁11.2g。则10min内CO的平均反应速率为
质铁11.2g。则10min内CO的平均反应速率为 
 (2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态: ① ②
① ②  (3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v) 和温度(T)的关系示意图中与铝热反应最接近的是 。
和温度(T)的关系示意图中与铝热反应最接近的是 。

 (4)写出氢氧化铝在水中发生酸式电离的电离方程式:
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:  欲使上述体系中
欲使上述体系中 浓度增加,可加入的物质是 。
浓度增加,可加入的物质是 。
在固定容积的密闭容器中,有可逆反应nA(g)+mB(g)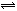 pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值,混合气体的密度;降温时,混合气体的平均相对分子质量;加入催化剂,气体的总物质的量;充入C,则A、B的物质的量。(增大、减小、不变、不确定)
pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值,混合气体的密度;降温时,混合气体的平均相对分子质量;加入催化剂,气体的总物质的量;充入C,则A、B的物质的量。(增大、减小、不变、不确定)
可逆反应3A(g) 3B(?)+C(?) △H>0达到化学平衡后,
3B(?)+C(?) △H>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
a.若B、C都是气体,气体的平均相对分子质量;
b.若B、C都不是气体,气体的平均相对分子质量;
c.若B是气体,C不是气体,气体的平均相对分子质量;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是态,C是态。
化学电池分为,,,其中碱性锌锰电池属于,铅蓄电池属于。
盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列的3个热化学反应方程式:
Fe203(s)+3CO(g)=2Fe(s)+3C02(g)△H=-24.8kJ/mol
Fe203(s)+1/3CO(g)="=" 2/3Fe3O4(s)+ 1/3C02(g)△H=-15.73kJ/mol
Fe304(s)+CO(g)==3FeO(s)+C02(g)△H=+640.4kJ/mol
试写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:______________________
【化学——选修有机化学基础】
聚酯纤维在服装、室内装饰和工业领域中有广泛应用。下图是合成某种聚酯纤维H的流程图。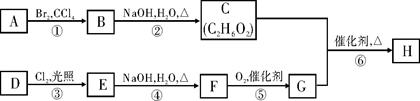
已知:A、D为烃,质谱图表明G的相对分子质量为166,其中含碳57.8%,含氢3.6%,其余为氧;G能与NaHCO3溶液反应且含有苯环;核磁共振氢谱表明E、G分子中均有两种类型的氢原子,且E分子中两种类型的氢原子的个数比为1:1。
(1)①、③的反应类型依次为、;
(2)B的名称为:;E的结构简式为:;
(3)写出下列化学方程式:
②;
⑥;
(4)F有多种同分异构体,写出同时符合下列条件的所有同分异构体的结构简式;
a.含有苯环且苯环上只有2个取代基
b.能与NaOH溶液反应
c.在Cu催化下与O2反应的产物能发生银镜反应