下列叙述不正确的是
| A.NaCl的摩尔质量是58.5g/mol |
B.将wg a%的NaCl溶液蒸发掉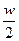 g水,得到2a%的NaCl溶液 g水,得到2a%的NaCl溶液 |
| C.将1体积cmol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2cmol/L |
| D.将5.85gNaCl晶体溶入1000mL水中,制得0.1mol/L的NaCl溶液 |
下列除去杂质的方法正确的是
| A.除去乙烷中少量的乙烯:光照条件下通入Cl2,使乙烯转化成液态二氯乙烷而与乙烷分离 |
| B.除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤,分液、干燥、蒸馏 |
| C.除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶 |
| D.除去乙醇中少量的乙酸:加足量生石灰,蒸馏 |
二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是HO-CH2CH2-O-CH2CH2-OH。下列有关二甘醇的叙述正确的是
| A.不能与金属钠发生反应 | B.能发生取代反应 |
| C.能溶于水,不溶于乙醇 | D.符合通式Cn H2nO3 |
可以用分液漏斗分离的一组液体混合物是
| A.溴和四氯化碳 | B.苯和溴苯 | C.水和硝基苯 | D.苯和汽油 |
下列关于有机化合物的说法正确的是
| A.乙醇和乙酸都存在碳氧双键 |
| B.甲烷和乙烯都可以与氯气反应 |
| C.高锰酸钾可以氧化苯和乙醛 |
| D.乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
下列说法中正确的是
| A.常温下,淀粉遇I-变蓝色 |
| B.油脂水解可得到氨基酸和甘油 |
| C.所有烷烃和蛋白质中都只存在碳碳单键 |
| D.淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖 |