密闭容器中的可逆反应3A(g)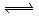 3 B+C ΔH="+890" kJ/mol(A的式量为120)随着温度升高,容器中气体相对平均分子质量减小,则下列判断正确的是( ).
3 B+C ΔH="+890" kJ/mol(A的式量为120)随着温度升高,容器中气体相对平均分子质量减小,则下列判断正确的是( ).
| A.若C为固体,则B一定是气体 |
| B.B和C一定都是气体 |
| C.若起始时往容器中投入18 g A,则反应吸收的热量为44.5 kJ |
| D.若起始时往容器中投入18 g A,则反应放出的热量为44.5 kJ |
相同质量的钠在下列情况下产生氢气最多的是
| A.放在足量水中 |
| B.放在足量盐酸中 |
| C.放在足量CuSO4溶液中 |
| D.用刺有小孔的铝,包好放入足量水底中 |
某溶液中可能含有H+、NH4+ 、Fe3+、Al3+、SO42-、CO32—等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示。
下列说法正确的是
| A.原溶液中含有的阳离子只有H+、Fe3+、Al3+ |
| B.原溶液中一定含有SO42-和Na+ |
| C.原溶液中含有的Fe3+和Al3+的物质的量之比为l:l |
| D.反应最后形成的溶液中溶质只有Na2SO4 |
下列离子方程式不正确的是
A.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3 2Cu2++CO2↑+3H2O 2Cu2++CO2↑+3H2O |
B.将Na2O2固体投入H218O中:2H218O+2Na2O2 4OH-+4Na++18O2↑ 4OH-+4Na++18O2↑ |
C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42—完全沉淀:2Ba2++NH4++Al3++2SO42—+4OH- Al(OH)3+NH3·H2O+2BaSO4 Al(OH)3+NH3·H2O+2BaSO4 |
D.向Na2FeO4溶液中加入稀硫酸产生氧气:4 FeO42—+20H+ 4Fe3++3O2↑+10H2O 4Fe3++3O2↑+10H2O |
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)△H="a" kJ/mol,在温度T1和T2时,分别将0.50molCH4和1.2molNO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g)△H="a" kJ/mol,在温度T1和T2时,分别将0.50molCH4和1.2molNO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化数据如下表:
下列说法不正确的是
| A.10 min内,T1时CH4的化学反应速率比T2时小 |
| B.T1<T2 |
| C.平衡常数:K(T1)<K(T2) |
| D.a<0 |
有如下装置.下列说法正确的是
| A.装置I和装置II中负极反应均是Fe - 2e-==Fe2+ |
| B.装置I和装置II中正极反应均是O2 + 2H2O + 4e-==4OH— |
| C.装置I和装置II中盐桥中的阳离子均向右侧烧杯移动 |
| D.放电过程中,装置I左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大 |