市场上有一种用于预防和治疗缺氧症状的便携式制氧器,利用过碳酸钠固体A(化学式为2Na2CO3·3H2O2)和灰黑色固体B(不溶于水)与水混合反应制得氧气。某同学对A、B两种物质进行探究,实验步骤及现象如下图所示。下列说法错误的是 
A. B在反应①中可能起催化作用 B.设计③的目的是制取氧气
C.第②步分离混合物的方法是过滤 D.白色沉淀D为CaCO3
下图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4·10H2O)在温度为T3 K 时开始分解为无水硫酸钠。现有142 g温度为T2 K的饱和硫酸钠溶液,当温度降为T1 K或升为T4 K(T4>T3)时析出晶体的质量相等,则温度为T4 K时Na2SO4的溶解度为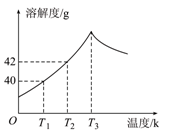
| A.小于40g | B.等于40g | C.等于42g | D.大于42g |
下列说法正确的是
| A.有阳离子的物质一定是离子晶体 | B.全部由极性键构成的分子一定是极性分子 |
| C.分子晶体的稳定性一定和共价键有关 | D.共价化合物不一定只有非金属元素组成 |
如图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是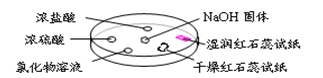
| 选项 |
实验现象 |
解释 |
| A |
浓盐酸附近产生白烟 |
NH3与浓盐酸反应产生了NH4Cl固体 |
| B |
浓硫酸附近无明显现象 |
NH3与浓硫酸不发生反应 |
| C |
氯化物溶液变浑浊 |
该溶液一定是AlCl3溶液 |
| D |
干燥红石蕊试纸不变色,湿润红石蕊试纸变蓝 |
氨气有碱性 |
以下实验能获得成功的是
| A.用醋酸钠晶体和碱石灰共热制甲烷 |
| B.将铁屑、溴水、苯混合制溴苯 |
| C.在苯酚溶液中滴人少量稀溴水出现白色沉淀 |
| D.将铜丝在酒精灯上加热后,立即伸人无水乙醇中,铜丝恢复成原来的红色 |
NA表示阿伏加德罗常数,下列叙述正确的是
A.32 g S8单质(右图)中含有的S—S键个数为8NA  |
| B.常温下,16gO2和O3的混合气体中所含氧原子数为2.5NA |
| C.1molMg在空气中完全反应生成MgO、Mg3N2转移电子数为2 NA |
| D.标准状况下,11.2 L的乙烯中含有的共用电子对数为NA |