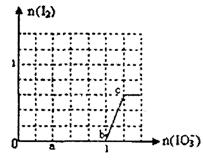
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2 .在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如右图所示.下列说法正确的是( )
| A.反应过程中的氧化产物均为SO3 |
| B.a点时剩余NaHSO3的物质的量为1.8 mol |
| C.c点时的还原产物可能是KI或NaI |
| D.当溶液中I¯与I2的物质的量之比为1:1时,加入的KIO3为1.2mol |
下列溶液中,与100 ml 0.5 mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是
| A.100 ml 0.5 mol/L MgCl2溶液 |
| B.200 ml 0.25 mol/L HCl溶液 |
| C.50 ml 1 mol/L NaCl溶液 |
| D.200 ml 0.25 mol/L CaCl2溶液 |
同温同压下,等质量的下列气体所占有的体积最大的是
| A.H2 | B.N2 | C.SO2 | D.Cl2 |
将标准状况下11.2L的HCl气体溶解于水配成1L溶液,所得溶液的浓度是
| A.2mol/L | B.1.5mol/L | C.1mol/L | D.0.5mol/L |
用NA表示阿伏德罗常数,下列叙述正确的是
| A.标准状况下,22.4LH2O含有的分子数为1 NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C.通常状况下,1 NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1 NA |
1.5mol空气在标准状况下占有的体积是
| A.22.4L | B.33.6L | C.44.8L | D.67.2L |