设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.1L mol·L‾1的硫酸铝溶液中含有的Al3+为2NA |
| B.1 L pH=1的硫酸溶液中含有的H+为0.2NA |
| C.标准状况下,22.4L的乙烷中含极性共价键的数目为7NA |
| D.常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 |
把aL硫酸铵和硝酸铵的混合液分成两等份,一份加入bmol 烧碱并加热,刚好把NH3全部赶出。另一份需消耗cmolBaCl2,沉淀反应刚好完全,原溶液中硝酸根离子的物质的量浓度为
A.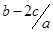 mol.l-1 mol.l-1 |
B.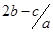 mol.l-1 mol.l-1 |
C.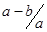 mol.l-1 mol.l-1 |
D.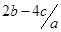 mol.l-1 mol.l-1 |
在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,每摩尔CuSO4能氧化P的物质的量为
| A.1/5 mol | B.2/5 mol | C.3/5mol | D.11/5 mol |
今有一包铁粉和铜粉混合粉末,为 确定其组成,现提供4 mol·L-1的FeCl3溶液(其它用品略),某合作学习小组同学的实验结果如下(假定反应前后溶液体积不变):
确定其组成,现提供4 mol·L-1的FeCl3溶液(其它用品略),某合作学习小组同学的实验结果如下(假定反应前后溶液体积不变):
| 组别 |
① |
② |
③ |
④ |
| V[FeCl3(aq)]/mL |
100 |
100 |
100 |
100[ |
| 混合粉末质量/g |
6 |
13.2 |
24 |
36 |
| 反应后剩余固体质量/g |
0 |
1.28 |
12.8 |
24.8 |
下列结论正确的是
A.第①组反应后溶液中c(Fe3+) =" 3.0" mol·L-1 B.第②组剩余固体是铁 和铜
和铜
C.第④组反应后的滤液中c(Fe2+) =" 6" mol·L-1 D.原混合粉末中n(Fe)∶n(Cu) = 3∶2
将0.51 mol铜与250 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2 混合气体在标准状况下的体积为11.2 L。待产生的气体全部释放后,向溶液中加入300 mL5 mol/L的NaOH溶液,恰好使溶液中的Cu2+ 全部转化成沉淀。则下列选项正确的是
| A.反应中转移电子1.0 mol | B.产生NO2气体0.26 mo1 |
| C.原HNO3浓度为8 mol/L | D.原HNO3浓度为2 mol/L |
下列各表述与示意图一致的是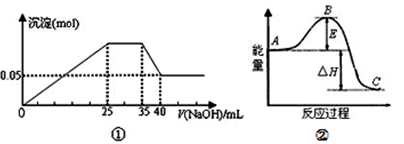
| A.图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图。则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:3:2 |
| B.图①中使用的NaOH的浓度为2 mol·L-1 |
C. 图②中曲线表示某反应过程的能量变化。若使用催化剂,B点会降低 图②中曲线表示某反应过程的能量变化。若使用催化剂,B点会降低 |
D.图②中物质A反应生成物质C,△H>0 |