氢气是一种清洁能源,可以通过多种方法制得。
(1) 工业上用水煤气法制氢气,有关化学方程式是:
反应一:C( s) + H2O(g)
s) + H2O(g)  CO(g) + H2(g) △H> 0
CO(g) + H2(g) △H> 0
反应二:CO(g) + H2O(g)  CO2(g) + H2(g) △H < 0
CO2(g) + H2(g) △H < 0
①若反应一在t℃时达到化学平衡状态,则此温度下该反应的的平衡常数表达式
K = ;
②在427℃时将CO 和H2O(g)各0.01mol通入体积为2升的密闭容器中反应,5分钟时达到平衡状态,该反应的平衡常数是9,则CO的转化率是 ,用CO的浓度变化表示的反应率速v(CO)是 mol /(L·min)。
(2)利用电解饱和食盐水也可制得氢气,下图为电解食盐水的示意图: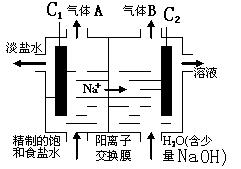
请回答:
① C1电极是 极(填“阴”或“阳”),C2电极的电极反应式是 。
②该电解反应的离子方程式是 ,
(3)通过下列方法也可以得到氢气。
已知: CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ·mol-1
1molCH4(g)与H2O(g)反应生成CO2(g)和H2(g)的反应热是 kJ·mol-1。
工业上可利用煤的气化产物(CO和H2)合成二甲醚(CH3OCH3)同时生成二氧化碳,其三步反应如下:
① 2H2 (g)+CO(g) 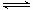 CH3OH (g) ΔH= -90.8 kJ·mol-1
CH3OH (g) ΔH= -90.8 kJ·mol-1
② 2CH3OH(g) 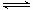 CH3OCH3(g)+H2O(g) ΔH= -23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH= -23.5 kJ·mol-1
③ CO(g)+H2O(g) 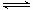 CO2 (g)+H2(g) ΔH= -41.3 kJ·mol-1
CO2 (g)+H2(g) ΔH= -41.3 kJ·mol-1
(1)总合成反应的热化学方程式为__________ _。
(2)一定条件下的密闭容器中,上述总反应达到平衡时,要提高CO的转化率,可以采取的措施是
__________(填字母代号)。
A高温高压 B加入催化剂 C减少CO2的浓度
D增加CO的浓度 E.分离出二甲醚
(3)已知反应②2CH3OH(g)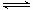 CH3OCH3(g)+H2O(g)在某温度下的平衡常数K = 400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)在某温度下的平衡常数K = 400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| c / mol·L-1 |
0.44 |
0.60 |
0.60 |
此时,v (正) _____ v (逆) (填“>”、“<”或“=”);达到平衡后,CH3OCH3的物质的量浓度是_____。
由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH、Mg2+、CO、Ba2+、SO。将该混合物溶于水后得澄清溶液,现取3份100 mL该溶液分别进行如下实验:
| 序号 |
试验内容 |
试验结果 |
| 1 |
加AgNO3溶液 |
有白色沉淀生成 |
| 2 |
加足量NaOH溶液并加热 |
收集到气体1.12L(已折算成标准状况下的体积) |
| 3 |
加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6.27g 第二次称量读数为2.33g |
试回答下列问题:
(1)根据实验判断混合物中一定存在的阴离子是,一定存在的阳离子是,一定不存在的离子是________,无法确定的离子是。
(2)写出实验2中发生反应的离子方程式。
为探索工业含铝、铁、铜合金废料的再利用,某同学设计的回收利用方案如下: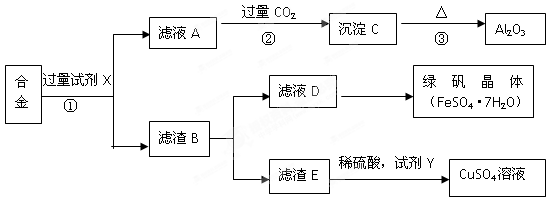
(1)写出反应①的离子方程式。
(2)步骤②中通入过量的CO2时生成沉淀的化学方程式为。
(3)检验滤液D是否含有Fe3+的最佳试剂为 (填序号)
A、KMnO4 B、NaOH C、氯水 D、KSCN
(4)若要从滤液D得到绿矾晶体,必须进行的实验操作步骤: 、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有 (填序号)
A.蒸发皿 B.石棉网 C.烧杯 D.玻璃棒
(5)试剂Y应该是一种 (填“氧化剂”或“还原剂”),它不可能是
A、H2O2 B、铁单质 C、O2
学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学反应。请按要求回答下列问题:
(1)写出下列反应的化学方程式。(注意反应条件并配平)
①镁带着火时,不能用液态CO2灭火剂来灭火的原因是。
②工业上用氯气和消石灰(氢氧化钙乳浊液)反应制取漂白粉。
(2)请你写出下列反应的离子方程式。
①胃舒平含有氢氧化铝,可用来治疗胃酸(盐酸)过多。
②电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(3)工业上生产半导体材料硅的流程如下: 
写出在制备粗硅时反应的化学方程式并标出电子转移的方向和数目:____________。
(4)铝热反应在工业生产中的重要用途之一是;小苏打在日常生活中的用途之一是,将小苏打和纯碱的混合物19.0g加热到恒重,测得固体质量为15.9g,则混合物中小苏打的质量分数为。
(15分)(1)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO  2CO2+N2
2CO2+N2
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中:
| 实验编号 |
T/℃ |
NO初始浓度mol/L |
CO初始浓度mol/L |
催化剂的比表面积m2/g |
| Ⅰ |
280 |
1.2×10-3 |
5.8×10-3 |
82 |
| Ⅱ |
124 |
|||
| Ⅲ |
350 |
124 |
①请在表格中填入剩余的实验条件数据。
②设计实验Ⅱ、Ⅲ的目的是。
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质。某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程。提供的装置: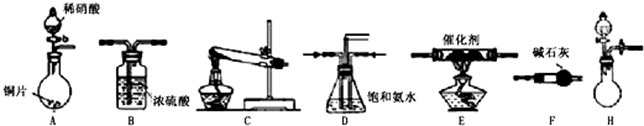
步骤一、NH3的制取
①所提供的装置中能快速、简便制取NH3的装置是:(填装置序号)。
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
| 试剂组合序号 |
固体试剂(g) |
NH3体积(mL) |
|
| a |
12.0gCa(OH)2(过量) |
10.8gNH4Cl |
2688 |
| b |
10.8g(NH4)2SO4 |
2728 |
|
| c |
12.0gNaOH(过量) |
10.8gNH4Cl |
3136 |
| d |
10.8g(NH4)2SO4 |
3118 |
|
| e |
12.0gCaO(过量) |
10.8gNH4Cl |
3506 |
| f |
10.8g(NH4)2SO4 |
3584 |
分析表中数据,实验室制NH3产率最高的是(填序号),其它组合 NH3产率不高的原因是。
步骤二、模拟尾气的处理选用上述部分装置,按下列顺序连接成模拟尾气处理装置: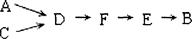
①A中反应的离子方程式:。
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:。
③D装置中的液体可换成(填序号)。
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是:。