将某稀硫酸和稀硝酸的混合溶液200mL。平均分成两等份。向其中一份中逐渐加入铜粉,最多能溶解19.2g;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸均只被还原为NO气体)。下列分析或结果不正确的是 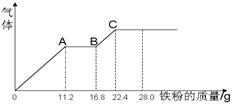
| A.第二份溶液中最终的溶质为FeSO4 |
| B.OA段产生的气体是NO,AB段的反应为 Fe+2Fe3+=3Fe2+,BC段产生的气体是H2 |
| C.原混合酸中NO-3的物质的量共为0.4mol |
| D.原混合酸中H2SO4的物质的量浓度为5mol·L-1 |
某有机物的结构为: ,它不具有的性质是①易溶于水②可以燃烧③能使酸性高锰酸钾溶液褪色④能跟KOH溶液反应⑤能跟NaHCO3溶液反应⑥能与溴水发生取代反应()
,它不具有的性质是①易溶于水②可以燃烧③能使酸性高锰酸钾溶液褪色④能跟KOH溶液反应⑤能跟NaHCO3溶液反应⑥能与溴水发生取代反应()
| A.①④ | B.①②⑥ | C.①⑤ | D.③⑤⑥ |
由溴乙烷制取乙二醇,依次发生反应的类型是()
| A.取代、加成、水解 | B.消去、加成、取代 |
| C.水解、消去、加成 | D.消去、水解、取代 |
下列纯净物中既能跟氢气反应,又能跟高锰酸钾溶液反应,但既不能跟溴水发生加成反应,又不能发生加聚反应的是()
| A.裂化汽油 | B.直馏汽油 | C.甲苯 | D.苯 |
下列四种烃的名称所表示的物质,命名正确的是()
| A.2-甲基-2-丁烯 | B.2-乙基丙烷 |
| C.3-甲基-2-丁烯 | D.2,2-二甲基-3-戊炔 |
某有机物C3H6O2的核磁共振氢谱中有两个共振峰,面积比为1︰1,该有机物的结构简式是()