材料是人类赖以生存的重要物质基础。材料种类很多,通常可分为金属材料、无机非金属材料(包括硅酸盐材料)、高分子合成材料及复合材料。
(1) ①合金是生活中常见的材料。某合金具有密度小、强度高的优良性能,常用于制造门窗框架。该合金中含量最高的金属为 (填元素符号)。
②铁锈的主要成分是 (填化学式),它是钢铁在潮湿的空气中发生 腐蚀的结果,其负极反应式为 。 ③玻璃是一种常用的硅酸盐材料。制备普通玻璃的原料有CaCO3、 和 (填化学式)。
③玻璃是一种常用的硅酸盐材料。制备普通玻璃的原料有CaCO3、 和 (填化学式)。
(2)聚苯乙烯是造成白色污染的物质之一,其结构简式为 ,则制取聚苯乙烯的单体是 。
,则制取聚苯乙烯的单体是 。
某芳香族酯类化合物甲的分子式为C14H10O5,1mol甲在酸性条件下水解后只生成一种产物乙,其物质的量为2mol,乙分子内苯环上只有两个邻位取代基。回答下列问题:
(1)写出有机物乙的结构简式。
(2)写出有机物甲和足量NaOH溶液反应的化学方程式。
(3)按下列要求写出和乙有不同 取代基的乙的同分异构体
取代基的乙的同分异构体
①苯环上有两个取代基。(写一种即可)
②苯环上有三个取代基。(写一种即可)
2008年北京残奥会吉祥物是以牛为形象设计的“福牛乐乐”(Funiulele)。有一种有机物的键线式也酷似牛形(下图所示) ,故称为牛式二烯炔醇(cowenyenynol)。回答下列有关该物质的问题:
,故称为牛式二烯炔醇(cowenyenynol)。回答下列有关该物质的问题: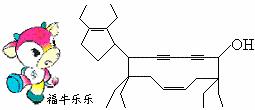
(1)“牛身”是由个碳原子形成的碳环。
(2)1 mol牛式二烯炔醇最多可跟mol Br2发生加成反应。
(3)该物质能否在浓硫酸、加热的条件下发生消 去反应?
去反应?
当甲烷的四个氢被甲基替换后,得到新戊烷,新戊烷的所有氢原子再被甲基替换得到新的烷烃,……
(1)请写出甲烷电子式。(2)请将新戊烷用系统命名法命名。
(3)试写出甲烷按上述方法连续进行三次甲基替换操作后所得烷烃的分子式
下列各组物质属于同系物的是,属于同分异物体的是;属于同位素的是 ,属于同素异形体的是,属于同一种物质的是。(填序号)
⑴O2和O3⑵氕和氚 ⑶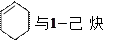 ⑷苯和对二甲苯
⑷苯和对二甲苯
⑸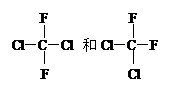 ⑹
⑹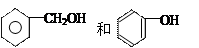 ⑺
⑺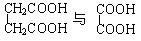
⑻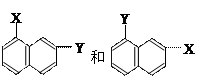 ⑼
⑼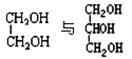 (10) 乙醇和乙醚
(10) 乙醇和乙醚
如图,A、B、C、D、E各代表碳、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D。请填空: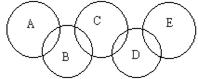
(1)写出下列物质的化学式:A ,B ,D 。
(2)写出下列反应的离子方程式:B+C: ,
,
(3)相连环物质间发生的反应中,氧化还原反应共有个。