25℃、101kPa 下:
①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414KJ/mol
②2Na(s)+O2(g)=Na2O2(s) △H2=-511KJ/mol
下列说法正确的是
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s)△H=-317kJ/mol |
用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的的是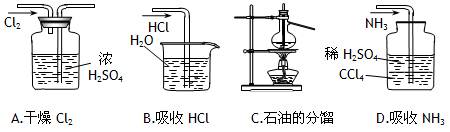
氢氧燃料电池已用于航天飞机。以30% KOH溶液为电解质溶液的这种电池在使用时的电极反应如下: 2H2+4OH--4e- = 4H2O O2+2H2O+4e- = 4OH-下列说法错误的是
| A.氧气通入正极发生氧化反应 |
| B.燃料电池的能量转化率不能达到100% |
| C.供电时的总反应为:2H2+O2 = 2H2O |
| D.产物为无污染的水,属于环境友好电池 |
化学研究和应用在资源的合理开发和利用中发挥着重要的作用。下列有关说法不正确的是
| A.煤的干馏、煤的气化和液化是目前实现煤的综合利用的主要途径 |
| B.酸雨、水华、温室效应等环境问题都与化石燃料有关 |
| C.海水淡化的方法主要有蒸馏法、离子交换法等 |
| D.石油裂化的目的是为了提高汽油的产量和质量 |
对于A2+3 B2= 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
A.v(B2)=" 0.8mol" /(L·s) B.v(A2)=" 0.4mol" /(L·s)
C.v(C)=" 0.6mol" /(L·s) D.v(B2)=" 4.2mol" /(L·min)
现代科技将 涂飞机表面,可以吸收和屏蔽雷达波和红外线辐射,从而达到隐形目的。下面列出该原子核内中子数与核外电子数之差的数据正确的是
涂飞机表面,可以吸收和屏蔽雷达波和红外线辐射,从而达到隐形目的。下面列出该原子核内中子数与核外电子数之差的数据正确的是
| A.41 | B.84 | C.125 | D.209 |