可逆反应①X(g)+2Y(g)
 2Z(g) 、②2M(g)
2Z(g) 、②2M(g) N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示: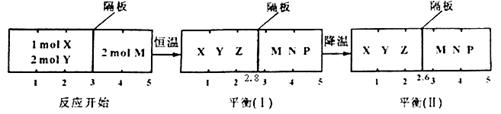
下列判断正确的是
| A.反应①的正反应是吸热反应 |
| B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15 |
C.达平衡(I)时,X的转化率为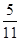 |
| D.在平衡(I)和平衡(II)中M的体积分数相等 |
根据元素的核电荷数,不能确定的是
| A.原子核内质子数 | B.原子核内中子数 |
| C.原子最外层电子数 | D.原子核外电子数 |
Na2SO4和NaCl溶液等体积混合后,Na+浓度为0.7mol·L-1,SO42-的浓度为0.2mol·L-1,则混合液中Cl-的浓度为
| A.0.15mol·L-1 | B.0.3mol·L-1 | C.0.45mol·L-1 | D.0.2mol·L-1 |
试管中盛有少量白色固体,可能是铵盐,检验的方法是
| A.加NaOH溶液,加热,滴入酚酞试剂 |
| B.加NaOH溶液,加热,滴入紫色石蕊试剂 |
| C.加NaOH溶液,加热,将干燥的红色石蕊试纸靠近试管口 |
| D.加NaOH溶液,加热,将湿润的红色石蕊试纸靠近试管口 |
某同学想要从碘的饱和水溶液中萃取碘,关于该实验的说法中不正确的是
| A.使用分液漏斗前应先检查其是否漏液 |
| B.可以选用苯、汽油、酒精和四氯化碳为萃取剂 |
| C.若用四氯化碳为萃取剂,将两种液体混合,充分振荡,静置,分层后,下层液体呈紫红色 |
| D.分层后,打开分液漏斗活塞,使全部下层液体沿承接液体的烧杯内壁流出,然后上层液体从漏斗上口倒出 |
用NA表示阿伏德罗常数,下列叙述正确的是
| A.标准状况下,22.4LH2O含有的分子数为1 NA |
| B.常温常压下,溶有1.06g Na2CO3的溶液中含有的Na+ 离子数为0.02 NA |
| C.通常状况下,1 NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1 NA |