下列实验操作正确的是
| A.分液:用分液漏斗分开汽油和植物油的混合溶液 |
| B.测pH:将pH试纸插入某溶液中,变色后与比色卡对比,读取pH |
| C.称量:用托盘天平准确称得(氢氧化钠固体+烧杯)总质量为25.56g |
| D.取量:用规格为10mL的量筒量取8.0mL液体 |
某化学反应的能量变化如下图所示。下列有关叙述正确的是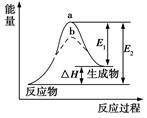
| A.该反应为放热反应 |
| B.E2可表示形成新的化学键所释放的能量 |
| C.该反应的反应热ΔH=E1-E2 |
| D.加入催化剂可同等程度的降低E1、E2 |
依据事实,写出下列反应的热化学方程式。
(1)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为________________________________________________。
(2)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热为-57.3kJ/mol): ___________________________________________________。
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4(1) △H1= -19.5kJ·mol-1
②N2H4(1) + O2(g)= N2(g) + 2 H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式________________。
下列热化学方程式中,正确的是
| A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H=-890.3 kJ·mol-1 |
B.由N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1热化学方程式可知,当反应中转移6NA电子时,反应放出的热量小于92.4 kJ 2NH3(g) △H=-92.4 kJ·mol-1热化学方程式可知,当反应中转移6NA电子时,反应放出的热量小于92.4 kJ |
| C.HCl和NaOH反应的中和热△H="-57.3" kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol-1 |
| D.在101 kPa时,4gH2完全燃烧生成液态水,放出571.6 kJ热量,氢气燃烧热的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H=-571.6 kJ·mol-1 |
根据热化学方程S (s) + O2 (g) = SO2 (g) △H = -297.23 kJ/mol (反应在298K,101kPa下发生)分析下列说法正确的是
| A.标况下,燃烧1mol S吸收的热量为297.23 kJ |
| B.S (g) + O2 (g) = SO2 (g) 放出的热量大于297.23 kJ |
| C.S (g) + O2 (g) = SO2 (g) 放出的热量小于297.23 kJ |
| D.形成1 mol SO2的化学键所释放的总能量大于断裂 1 molS (s)和 1mol O2 (g)的化学键所吸收的总能量 |
下列说法正确的是
| A.在101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 |
| B.酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
| C.燃烧热或中和热都是反应热的种类之一 |
| D.其他条件一样时,氢气与氧气反应生成液态水和气态水时所放出的热量相等 |