下列实验操作正确的是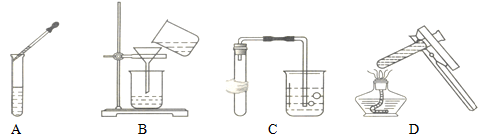
下列物质的性质与所对应的用途没有关系的是
| A.氧气助燃——焊接金属 | B.氮气的化学性质稳定——作保护气 |
| C.铜能导电——可作电线 | D.二氧化碳能与水反应——人工降雨 |
家庭生活中处处都有物质变化,下列发生在家庭生活中的变化属于物理变化的是
| A.鲜牛奶变质 | B.用粮食酿酒 | C.钢丝球刷碗 | D.洁厕精除垢 |
某班同学用下图装置测定空气里氧气的含量,实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的五分之一,乙同学的广口瓶内水面上升明显大于瓶内空气体积的五分之一。下列对这两种现象解释合理的是()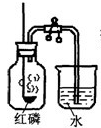
①甲同学可能使用的红磷量不足
②甲同学可能塞子塞慢了
③乙同学使用的装置可能气密性较差
④乙同学可能没有夹紧弹簧夹,红磷燃烧时瓶内空气受热逸出
| A.全部 | B.①④ | C.②③ | D.①③④ |
某学生取液体,开始时视线与量筒内液体的凹液面最低处相平读数为30mL,将液体倒出一部分后,俯视量筒内剩余液体读数为20mL,则该同学实际倒出的液体体积为()
| A.大于10mL | B.小于10mL | C.等于10mL | D.无法确定 |