(8分,每空2分)实验室要配制500mL2.0mol·L-1氯化钠溶液。请回答下列问题:
(1)应用托盘天平称取NaCl固体 g;
(2)下列仪器中,配制时一定不会用到的是(填字母) ;
A.量筒 B.500 mL烧瓶
C.胶头滴管 D.500mL容量瓶
(3)除上述(2)中用到的仪器外,还缺少的玻璃仪器有 ;
(4)右图所示是某同学配 制溶液时最后两个步骤,按其操作定容,对所配溶液浓度有何影响? (填“偏高”、”偏低”或“无影响”);
制溶液时最后两个步骤,按其操作定容,对所配溶液浓度有何影响? (填“偏高”、”偏低”或“无影响”);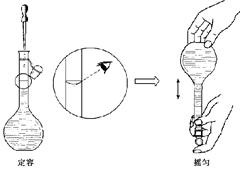
某同学欲配制450mL 0.1mol/L的碳酸钠溶液,试根据所学回答下列问题。
(1)若采用5mol/L的碳酸钠溶液配制溶液,需要用到碳酸钠溶液的体积为。
(2)若用碳酸钠固体配制,一定会用到的仪器有________________________
A.450ml容量瓶 B.500 ml容量瓶 C.量筒 D.胶头滴管
E.烧杯 F.玻璃棒 G.托盘天平
(3)欲准确配制所需溶液,下列称量质量正确的是()
A.称Na2CO3 4.8克 B.Na2CO3 5.3克
C.称Na2CO3·10H2O 12.87克 D.称Na2CO3·10H2O 14.30克
(4)若在配溶液的过程中用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是________(填序号)。
A.吸出多余液体,使凹液面与刻度线相切
B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的碳酸钠固体
D.重新配制
(5)下列操作可能导致结果偏高的是。
A.转移后没有洗涤烧杯
B.定容时俯视
C.定容时仰视
D.称取的Na2CO3溶液中混有少量Na2CO3·10H2O
E.配溶液前用碳酸钠溶液润洗容量瓶
(9分)某化学兴趣小组对生石灰与水反应是显著放热反应进行了实验探究,在除了用手触摸试管壁感觉发热外,还设计了下列几个可行性方案。
甲方案:将温度计与盛放有生石灰的小试管用橡皮筋捆绑在一起,放入有水的小烧杯中,用胶头滴管向小试管中缓缓滴入水,看到的现象是,说明反应放热。(下列装置中支撑及捆绑等仪器已略去)
乙方案:将盛放有生石灰的小试管插入带支管的试管中,支管接①或②,用胶头滴管向小试管中缓缓滴入水,看到的现象是(接①),(接②),说明反应放热。
丙方案:用胶头滴管向盛放有生石灰且带支管的试管中滴加水,支管接的导管中盛适量无水硫酸铜粉末,看到的现象是,说明反应放热,其原因是。
(8分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,体积已换算成标准状态)):
 时间(min) 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大, 原因是。
原因是。 (2)哪一段时段的反应速率最小,原因是
(2)哪一段时段的反应速率最小,原因是 。
。 (3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)。
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)。 (4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
| A.蒸馏水 | B.NaCl溶液 | C.Na2CO3溶液 | D.CuSO4溶液 |
 你认为可行的是(填编号)。
你认为可行的是(填编号)。
某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由 。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1H2SO4、3% H2O2、6 mol·L-1HNO3、0.01 mol·L-1KMnO4、NaOH稀溶液、0.1 mol·L-1Kl、20% KSCN、蒸馏水。
提出合理假设
假设1: ;
假设2: ;
假设3: 。
设计实验方案证明你的假设(不要在答题卡上作答)
实验过程
根据②的实验方案,进行实验。请在答题卡上按下表格式写出实验操作步骤、预期现象与结论。
| 实验操作 |
预期现象与结论 |
| 步骤1: |
|
| 步骤2: |
|
| 步骤3: |
|
| … |
现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)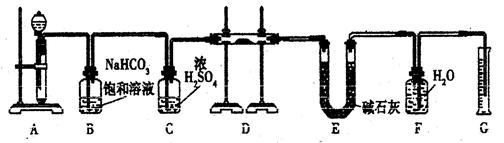
回答下列问题:
(1)装置A中液体试剂选用,理由是。
(2)装置B的作用是。
装置C的作用是。
装置E中碱石灰的作用是。
(3)装置D中发生反应的化学方程式是。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为。