鉴别下列各组物质,按要求回答问题。
(1)稀硫酸、稀盐酸
①可选用鉴别的试剂有(填编号) ▲ (多选题) 。
A.BaCl2溶液 B.Ba(NO3)2溶液 C.Ba(OH)2溶液
②鉴别反应的离子方程式: ▲ 。
(2)饱和碳酸钠溶液 、澄清石灰水
、澄清石灰水
①可选用鉴别的试剂有(填编号) ▲ (多选题) 。
a.盐酸 b.硫酸 c.硝酸 d.BaCl2溶液 e.NaCl溶液
②依次写出鉴别中有明显现象的反应的离子方程式: ▲ 。
(28分,每空2分)下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
 主族 主族周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
A |
B |
||||||
| 2 |
D |
E |
F |
J |
||||
| 3 |
C |
G |
H |
I |
(1)金属性最强的元素名称是,性质最稳定的元素是(填化学式)
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为;该物质溶于水后的溶液呈________性(填“酸”、“碱”或“中”),原因是
(用相关方程式解释)。
(3)X微粒核外有10个电子,当获得3个电子时呈电中性,写出该粒子的结构示意图,X元素在周期表中的位置:,X最高价氧化物的水化物与过量NaOH反应的离子方程式:
(4)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的________(填字母序号)元素组成的,用化学方程式表示吸收原理:
。飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体结构式为。
(5)用电子式表示H 与C形成化合物的过程:
(6)J和I氢化物的沸点较高的是(用化学式),原因是。
下图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从两极通入燃料电池时,便可在闭合回路中不断地产生电流.这被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高率的特点。试回答下列问题:
(1)图中通过负载(负载是指用电器)的电子流动方向(填“向左”或“向右”),负极发生反应。
(2)写出氢氧燃料电池工作时的电极反应式负极:,正极:,
(3)电池工作时,负极区的PH值(填“增大”或“不变”或“减小”)。
已知X为中学化学中的一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的组成元素的离子半径是第三周期元素中离子半径最小的。N的最高价氧化物是耐火材料,它的晶体硬度很大,常做手表的轴承;H为气体单质,D为无色气体,在空气中会出现红棕色。各物质的转化关系如下图(部分反应产物已略去)。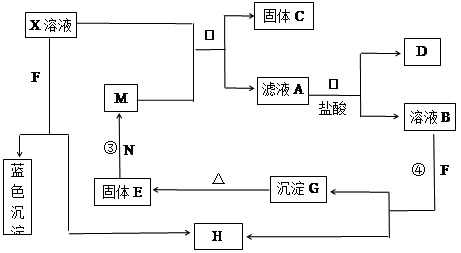
请回答下列问题:
(1)X的化学式为;F的电子式为 。
(2)反应②的离子方程式为_______________________________________________。
反应③的化学方程式为_______________________________________________。
(3)若向100 mL盐X的溶液中加入10 g金属单质M的粉末,充分搅拌后,过滤,烘干
得10.16g固体C。则滤液A中溶质的物质的量浓度为________________________。(假设体积不变)
在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H2⇌2NH3已知加入1 mol N2、4 mol H2时,达到平衡后生成a mol NH3(见表中已知项),在相同温度和压强下保持平衡后各组分体积分数不变,对下列编号①~③的状态,填写表中空白。
| 已知编号 |
始态的物质的量(mol) |
平衡时NH3的 物质的量(mol) |
||
| N2 |
H2 |
NH3 |
||
| 已知 |
1 |
4 |
0 |
a |
| ① |
1 |
0.5a |
||
| ② |
1.5 |
6 |
0 |
|
| ③ |
m |
n( n≥4m) |
如下图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始时A、B的体积均为a L,在相同温度和有催化剂条件下,两容器中各自发生反应:
X(g)+Y(g) ⇌2Z(g)+W(g)(正反应为放热反应)达到平衡时A容器的体积为1.2a L。
(1) A中X的转化率αA=
(2) A、B中X的转化率αA αB(填 >、< 或 = )
(3)打开K,一段时间又达到平衡时A的体积为L(连通管中气体体积忽略不计)
(4)在(3)达到平衡后,同时等幅升高A、B的温度,达到新平衡后,A的体积(填变大、变小或不变)