铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下图所示,请回答有关问题: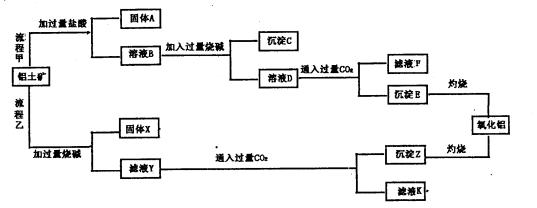
(1)流程乙加入烧碱后发生反应 的离子方程式: .
的离子方程式: .
(2)溶液D到沉淀E发生的离子方程式: 。
(3)验证滤液B含Fe3+,可取少量滤液并加入 。
(4)滤液K中溶质的主要成份是 (填化学式)。
下图表示某些物质间转化关系(部分反应条件省略)。其中A为黑色固体氧化物;E为绿色固体;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;
请回答下列问题:
(1)请判断X的化学式:。
(2)反应①中A物质的作用是。
(3)反应①、⑤的化学方程式:①;⑤。
(4)在日常生活中为防止反应②的发生,可采取的措施是(写一点即可)。
在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应。例如:2Na+C12=2NaCl,反应前后Na、C1元素的化合价发生了变化,该反应是氧化还原反应。
⑴含有高价态元素的化合物,在反应前后元素的化合价降低,通常具有氧化性。如:氯化铁溶液能和单质铜反应生成氯化铜和另一种铁的氯化物。该反应的化学方程式可表示为____________________________________;该反应中,_________元素的化合价发生了变化,反应物中表现出氧化性的物质是___________。
⑵向上述反应后的溶液中加入过量的锌粉充分反应后过滤,则滤液中的溶质是______。
〖反思与评价〗
⑶有人认为复分解反应一定不属于氧化还原反应,请你也从化合价角度解释原因____________________________________________________。
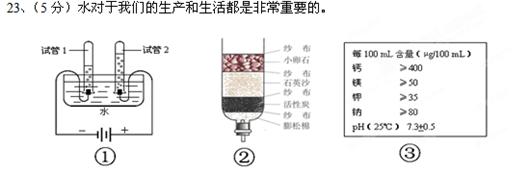
(1)图①所示电解水的实验中,试管(填“1”或“2”)中收集的气体是氧气。
(2)小刚要净化收集的雨水,自制了一个简易净水器(如图②所示),其中小卵石、
石英沙和膨松棉的作用是。
(3)某塑料瓶装矿泉水标签如图③所示,饮用该矿泉水,可以为人体提供_________种营养素。塑料瓶轻便卫生,可回收再利用。其所用材料不属于 。
。
A. 合成材料B.有机高分子C.有机物D.合金
(4)我们应当珍惜每一滴水,下列做法不利于节约用水的是。
A.洗菜的水用来浇花B.使用节水龙头
C.用不间断的流水冲洗碗筷D.洗手擦肥皂时,关上水龙头
22、福岛核泄漏引发全球关注核安全。
(1)核电站提供了世界约17%的电能,核能的开发和利用,有效地缓解了化石燃料贮量不足带来的能源危机。化石燃料是指煤、和 天然气。
天然气。
(2)福岛核电站爆炸的元凶是氢气,氢气燃烧爆炸时的化学方程式为。核电站的氢气主要来源于燃料原件上的锆(Zr)高温下与水反应,生成氧化锆(ZrO2)和氢气,该反应的化学方程式为。
(3)核电站利用核燃料铀—235发生核裂变产生的能量发电。放射性碘( )是核裂变产物之一。
)是核裂变产物之一。 原子核内有53个质子,78个中子,关于
原子核内有53个质子,78个中子,关于 ,下列说法正确的是__________(填序号)。
,下列说法正确的是__________(填序号)。
① 原子核外电子数为78②
原子核外电子数为78② 的相对原子质量约为131
的相对原子质量约为131
③ 放射性碘和稳定性碘属于同种元素④ 碘是人体必需的微量元素
(4) 一旦被人体吸入会引发甲状腺疾病。服用含碘元素的物质可封闭甲状腺,让放射性碘无法“入侵”。我国规
一旦被人体吸入会引发甲状腺疾病。服用含碘元素的物质可封闭甲状腺,让放射性碘无法“入侵”。我国规 定在食盐中添加碘元素的标准为20-40mg/kg,若要达到防御
定在食盐中添加碘元素的标准为20-40mg/kg,若要达到防御 辐射的作用,一次需补充碘元素100mg。按每人每天食用10g加碘盐,则我们每天最多能从碘盐中吸收 ______ mg碘元素。
辐射的作用,一次需补充碘元素100mg。按每人每天食用10g加碘盐,则我们每天最多能从碘盐中吸收 ______ mg碘元素。
(7分)在宏观、微观和符号之间建立联系是化学学科特点。
(1)在水、铜、氯化钠3种物质中,由离子构成的是。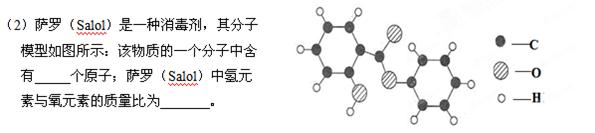
 A、B、C、D中属于单质的是(填化学式,下同);属于氧化物的是。
A、B、C、D中属于单质的是(填化学式,下同);属于氧化物的是。
(4)某粒子的结构示意图为 ,当x-y=8时,该粒子为________。
,当x-y=8时,该粒子为________。
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是__________。
A.NO和O2 B.CO和N2 C.SO2和CO2 D.PO43- 和SO42-