(1)实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2 O(1) △H<0
O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应的电极反应式为 。
(3)电解原理在化学工业中有着广泛的应用。
现将你设计的原电池通过导线与下图中电解池相连,其中,a为电解液,X和Y是两块电极板,则: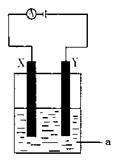
① 若X和Y均为惰性 电极,a为CuSO4溶液
电极,a为CuSO4溶液
则阳极的电极反应式为 ,电解时的化学反应方程式为 ,通过一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电 极反应式为
极反应式为
③若用此装置电解精炼铜, 做阳极,电解液CuSO4的浓度 (填“增大”、“减小”或“不变”)。
④若用此装置在铁制品上镀铜,铁制品做 ,电镀液的浓度 (填“增大”、“减小”或“不变”)。
A、B、C、D四种短周期元素。原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)写出下列元素的名称:A_______,B,C_______,D。
(2)D的质子数和中子数相等,D的原子组成符号为,它的最高价为_________价。
(3)用电子式表示A、B两元素形成AB2的过:;
写出C2B2的电子式。
(4)氢元素与B、D 均可以形成原子个数比为2:1的化合物,H2B的熔沸点高于H2D的原因是。
(5)写出甲和A的最高价氧化物反应的化学方式:。
某气态烷烃A的密度是相同状况下H2的29倍,则:A的分子式为,请写出A所有同分异构体的结构简式,其一氯取代产物共有种。
铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式: _______________________________
(2)若将(1)中的反应设计成原电池,请在方框内画出原电池的装置图,标出正、负极及材料、电解质溶液并写出电极反应式。 
正极反应____________________________;
负极反应____________________________。
(3)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答下列问题: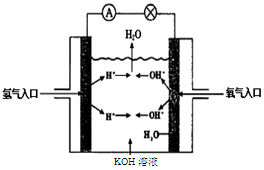
①负极反应式为溶液PH(填“增大”、“不变”或“减小”)。
②该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2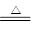 2LiHⅡ.LiH+H2O=LiOH+H2↑
2LiHⅡ.LiH+H2O=LiOH+H2↑
反应Ⅰ中的还原剂是,7 gLi可吸收标况下H2L,此时转移电子moL。
完成下列方程式(要注明反应条件)。
①甲烷与氯气反应制一氯甲烷:________________________②乙烯使溴水褪色:_______________
③苯和液溴混合加铁粉 :__________________④制备乙酸乙酯:_________________________________
有下列几组物质或微粒:
| A.11H和21H | B.甲烷和乙烷 | C.红磷和白磷 | D.金刚石、石墨和C60 |
E.丁烷和异丁烷F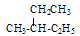 和
和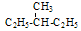 其中,属于同分异构体的是______;属于同位素的是______;属于同素异形体的是_______;属于同一种物质的是________;属于同系物的是_________。(填字母编号)
其中,属于同分异构体的是______;属于同位素的是______;属于同素异形体的是_______;属于同一种物质的是________;属于同系物的是_________。(填字母编号)