用乙烯在硫酸催化下的水化法合成乙醇,事实上经过下列步骤:首先在较低温度下用浓硫酸吸收乙烯: CH2=CH2 +H2SO4(浓) → CH3CH2OSO3H (Ⅰ),然后生成物(Ⅰ)再进一步吸收乙烯:CH3CH2OSO3H + CH2=CH2→(CH3CH2O)2SO2(Ⅱ),再加入水,(Ⅰ)和(Ⅱ)都与水反应生成乙醇:CH3CH2OSO3H +H2O → CH3CH2OH + H2SO4 ;(CH3CH2O)2SO2 +2H2O → 2CH3CH2OH + H2SO4
→ CH3CH2OSO3H (Ⅰ),然后生成物(Ⅰ)再进一步吸收乙烯:CH3CH2OSO3H + CH2=CH2→(CH3CH2O)2SO2(Ⅱ),再加入水,(Ⅰ)和(Ⅱ)都与水反应生成乙醇:CH3CH2OSO3H +H2O → CH3CH2OH + H2SO4 ;(CH3CH2O)2SO2 +2H2O → 2CH3CH2OH + H2SO4
下列叙述中正确的是
①化合物(Ⅰ)、(Ⅱ)都属于酯类 ②生成(Ⅰ)、(Ⅱ)的反应都属于加成反应
③生成醇的反应都属于取代反应
| A.①②③ | B.只有②③ | C.只有① | D.只有①③ |
在一固定容积的密闭容器中加入2 L X气体和3 L Y气体,同时发生如下反应:nX(g)+3Y(g) 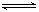 2R(g) +Q(g),反应达到平衡时,测知X和Y的转化率分别为30%和60%。问化学方程式中的n值是()
2R(g) +Q(g),反应达到平衡时,测知X和Y的转化率分别为30%和60%。问化学方程式中的n值是()
| A.1 | B.2 | C.3 | D.4 |
在某条件下,容器中有如下平衡反应:A +4B  2C + D + Q,此时,A,B,C的物质的量均为amol,而D的物质的量为dmol。改变a的取值,再通过改变反应的条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2与2d之间变化,则a的取值范围应是__________________________(用a和d的关系式表示)。
2C + D + Q,此时,A,B,C的物质的量均为amol,而D的物质的量为dmol。改变a的取值,再通过改变反应的条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2与2d之间变化,则a的取值范围应是__________________________(用a和d的关系式表示)。
在一定条件下,将X和Y两种气体按不同比例充入密闭容器中,并保持其他条件不变,测得平衡时X和Y的转化率与起始状态X与Y的物质的量之比有如右图所示的关系,则X和Y反应的方程式是()
A.2X+Y Z Z |
B.X+2Y Z Z |
C.3X+Y 2Z 2Z |
D.2X+Y 2Z 2Z |
加热N2O5按下式分解:N2O5 N2O3+O2,N2O3又按N2O3
N2O3+O2,N2O3又按N2O3 N2O+O2分解,在容积为1L的密闭容器中,将4molN2O5加热至t℃,达平衡时,氧气的浓度为4.5mol/L,N2O5的平衡浓度为1.7mol/L,则t℃时N2O5的平衡浓度应为()
N2O+O2分解,在容积为1L的密闭容器中,将4molN2O5加热至t℃,达平衡时,氧气的浓度为4.5mol/L,N2O5的平衡浓度为1.7mol/L,则t℃时N2O5的平衡浓度应为()
| A.0.9mol/L | B.1.5mol/L | C.2.38mol/L | D.2.88mol/L |
在2L的密闭容器中,把4molA和2molB混合,在一定条件下发生反应:3A(g)+2B(g)  xC(g)+2D(g),2min后达到平衡时生成1.6molC,又测得反应速率v(D)=0.2mol/(L·min)。下列说法正确的是()
xC(g)+2D(g),2min后达到平衡时生成1.6molC,又测得反应速率v(D)=0.2mol/(L·min)。下列说法正确的是()
A.消耗B 0.08mol B.x="4"
C.A的平衡浓度是1.4mol/L D.平衡时气体压强是原来的0.94倍