一定量的氢气在氯气中燃烧,所得混合物用100ml 3.00mo l/L的NaOH溶液(密度为1.2g/ml)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05 mol(溶液中只含NaCl和NaClO两种溶质)。则下列有关说法不正确的是
l/L的NaOH溶液(密度为1.2g/ml)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05 mol(溶液中只含NaCl和NaClO两种溶质)。则下列有关说法不正确的是
| A.原NaOH溶液的质量分数为10.0% |
| B.所得溶液中Cl-的物质的量为0.25 mol |
| C.与NaOH反应的氯气为0.15 mol |
D.所用氯气和参加反应的氢气的物质的量之比 为3 为3 ﹕2 ﹕2 |
下面三个方法都可以制氯气:
MnO2+4HCl(浓)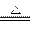 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
2KMnO4+16HCl(浓)====2KCl+2MnCl2+8H2O+5Cl2↑
4HCl(g)+O2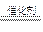 2Cl2+2H2O(g)
2Cl2+2H2O(g)
则三种氧化剂由强到弱的顺序是( )
| A.O2 MnO2 KMnO4 | B.KMnO4 MnO2 O2 |
| C.MnO2 KMnO4 O2 | D.O2 KMnO4 MnO2 |
根据下列反应的化学方程式判断下列物质氧化性强弱排序正确的是( )
①2FeCl3+Cu====2FeCl2+CuCl2
②CuCl2+Fe====FeCl2+Cu
| A.CuCl2>FeCl2>FeCl3 | B.FeCl3>FeCl2>CuCl2 |
| C.CuCl2>FeCl3>FeCl2 | D.FeCl3>CuCl2>FeCl2 |
下列粒子氧化性最强的是( )
| A.H+ | B.Fe2+ | C.Cu2+ | D.Ag+ |
下列说法正确的是( )
①非金属只能作氧化剂②活泼的金属只能作还原剂
③金属阳离子都具有氧化性④金属阳离子只能作还原剂
| A.①② | B.②③ | C.③ | D.④ |
已知①2CuO+C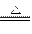 2Cu+CO2↑;②2Mg+CO2
2Cu+CO2↑;②2Mg+CO2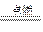 2MgO+C,由此得出下列结论正确的是( )
2MgO+C,由此得出下列结论正确的是( )
| A.还原性:Mg>C>Cu | B.还原性:Mg>Cu>C |
| C.氧化性:CuO>CO2>MgO | D.氧化性:CuO>MgO>CO2 |