下列各组离子中,在碱性溶液里能大量共存,且溶液为无色透明的是( )
A K+、MnO4–、Cl–、SO42– B Na+、OH–、NO3–、CO32–
C Na+、H+、NO3–、SO42– D Na+、Cu2+、NO3–、Cl–
下列关于Na2CO3的说法不正确的是
| A.Na2CO3与石灰水混合有白色沉淀生成 |
| B.Na2CO3与CaCl2溶液混合有白色沉淀生成 |
| C.Na2CO3俗称纯碱是因为它是碱 |
| D.Na2CO3可以与盐酸反应放出CO2 |
金属钠分别与下列溶液反应时,既有气体又有沉淀产生的是
| A.氯化铵 | B.碳酸氢钠 | C.氯化钡 | D.硫酸铜 |
下列表示物质结构的化学用语或模型正确的是
| A.碳元素位于周期表中第二周期ⅥA族 |
B.HF的电子式: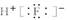 |
C.Cl-离子的结构示意图: |
| D.质量数为39的钾原子1939K |
对于某些离子或物质的检验所用试剂或方法不正确的是
| A.某溶液中加入盐酸产生气体,则其中一定含有CO32- |
| B.用焰色反应检验钠元素的存在 |
| C.用氢氧化钠溶液和湿润的红色石蕊试纸检验NH4+ |
| D.用盐酸和氯化钡溶液检验 SO42- |
下列分离物质的方法中,不正确的是
| A.利用蒸发的方法从石油中分离出汽油和煤油 |
| B.利用分液的方法将水和苯分离开来 |
| C.利用结晶的方法除去硝酸钾中混有的少量氯化钾 |
| D.利用过滤的方法除去水中的泥沙 |