下列对城市废弃物中生物质能利用不合理的是( )
| A.把废弃物进行生物化学置换获取CH4 |
| B.对废弃物进行处理后焚烧,利用产生的热能供暖和发电 |
| C.把废弃物拉到乡下找个地方填埋掉 |
| D.让废弃物在一定条件下发生化学反应为,产生热值较高的可燃性气体 |
铁路氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,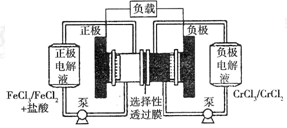
工作原理为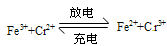 下列说法一定正确的是
下列说法一定正确的是
| A.电池充电时,阴极的电极反应式为Cr3++e-=Cr2+ |
| B.电池放电时,负极的电极反应式为Fe2+-e-=Fe3+ |
| C.电池放电时,Cl-从负极穿过选择性透过膜移向正极 |
| D.电池放电时,电路中每通过0.1mol电子,Fe3+浓度降低0.1mol·L-1 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH+O2=CH3COOH+H2O |
| D.正极上的反应式:O2+4e—+2H2O=4OH- |
关于下列各装置图的叙述不正确的是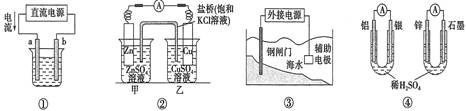
| A.用图①装置精炼铜,a极为粗铜,电解质溶液为CuSO4溶液 |
| B.图②装置中盐桥中的Cl-移向乙烧杯 |
| C.图③装置中钢闸门可与外接电源的负极相连受到保护 |
| D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同 |
下列说法正确的是
| A.25℃时,pH为9的Na2CO3溶液和pH为5的NaHSO4溶液中,水的电离程度相同 |
| B.在含Al3+的KNO3溶液中,可通过加热法除去Al3+,证明盐的水解是吸热反应 |
| C.已知HF的酸性比HCN的酸性强,则等体积等浓度NaF和NaCN两溶液中阳离子的物质的量之和相等 |
| D.等物质的量浓度的①NH4Cl ②NH4HSO4③Na2S ④NaNO3⑤(NH4)2SO4,其pH由大到小的排列为③>④>⑤>①>② |
常温下,某一元弱酸的电离平衡常数为:Ka=10-6,对于0.01mol·L-1的该酸,下列说法不正确是
| A.该弱酸溶液的pH=4 |
| B.加入NaOH溶液后,弱酸的电离平衡向右移动,但Ka不变。 |
| C.加入等体积的0.01mol·L-1NaOH溶液后,所得的溶液的pH<7 |
| D.该弱酸的钠盐溶液一定会发生水解,常温下,其水解平衡常数Kh=10-8 |