可逆反应H2(g)+I2(g)  2HI(g)达到平衡时的标志是( )
2HI(g)达到平衡时的标志是( )
| A.混合气体密度恒定不变 |
| B.混合气体的颜色不再改变 |
| C.H2、I2、HI的浓度相等 |
| D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
下列事实不能用勒夏特列原理解释的是
A.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B.合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 |
C.反应CO(g)+NO2(g) CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深 |
D.对于2HI(g) H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深 |
升高温度,下列数据不一定增大的是
| A.化学反应速率 | B.水的离子积常数Kw |
| C.化学平衡常数 | D.弱酸的电离平衡常数Ka |
可逆反应aA(g)+bB(g) cC(g)+dD(g)符合下图。则下列叙述正确的是
cC(g)+dD(g)符合下图。则下列叙述正确的是

| A.a+b>c+d;正反应放热 |
| B.a+b<c+d;正反应吸热 |
| C.a+b<c+d;正反应放热 |
| D.a+b>c+d;正反应吸热 |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)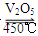 2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是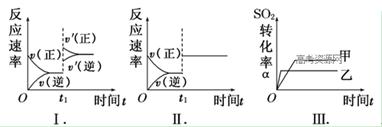
| A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B.图Ⅱ表示的是t1时刻加入催化剂对反应速率的影响 |
| C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化剂效率比乙高 |
| D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
可以证明可逆反应N2+3H2 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
①一个N≡N断裂的同时,有3个H-H键断裂②一个N≡N键断裂的同时,有6个N-H键断裂③其它条件不变时,混合气体平均摩尔质量不再改变④保持其它条件不变时,体系压强不再改变⑤NH3%、N2%、H2%都不再改变⑥恒温恒容时,密度保持不变⑦正反应速率υ(H2) =" 0.6" mol/(L·min),逆反应速率υ(NH3) =" 0.4" mol/(L·min)
| A.全部 | B.②③④⑤⑦ | C.①③④⑤ | D.③⑤⑥⑦ |