C、N、S元素都是生命体的重要组成元素,它们在自然界的平衡已受到较大的破坏。C、N、S元素在地球大气圈、岩石圈、水系、生物圈的循环过程中会产生的物质是( )
①HNO3 ②CO2 ③糖类 ④CH4
A.② B.②③ C.②③④ D.①②③④
最近,科学家冶炼出纯度高达99.999 %的铝,你估计它具有性质是()
| A.熔点比铁铝合金小 |
| B.在冷、浓HNO3中可以钝化 |
| C.在空气中放置容易生锈,进而被腐蚀 |
| D.当它与铁的粉碎粒度相同时,与4mol/L盐酸反应速率比纯铁大 |
下列各图均能表示甲烷的分子结构,哪一种更能反映其真实存在状况 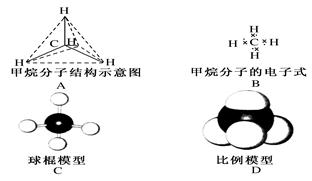
下列叙述正确的是
| A.电解精炼金属时,含杂质的粗金属做阳极,与电源正极相连 |
| B.电解池中金属导线中电子由电源的负极流向电解池的阳极,从电解池的阴极流向电源的正极 |
| C.在电解池中,电解质溶液中的阴离子向阴极移动,阳离子向阳极移动 |
| D.在电解精炼金属过程中,电解质溶液的成分不发生任何变化 |
在25℃时将pH=11 的NaOH 溶液与pH=3 的CH3COOH溶液等体积混合后下列关系式中正确的是
| A.c (Na+)=c(CH3COO-)+c(CH3COOH) | B.c(CH3COOH) =c(CH3COO-) |
| C.c (Na+) > c (CH3COO-)>c(OH-)>c(H+) | D.c (CH3COO-)>c(Na+)>c(H+)>c(OH-) |
在25℃时,将两个铜电极插入到一定的Na2SO4饱和溶液中,通直流电电解并不断搅拌,当阴极上收集到amol的气体的同时,溶液中析出了bmol的结晶水合物Na2SO4·10H2O,若保持温度不变,则所剩溶液中溶质的质量分数是
| A.71b/18a | B.71b/36a | C.71b/(161b+18a) | D.71b/(161b+9a) |