标准状况下将VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为ρ g/mL,质量分数为w,物质浓度为c mol/L,则下列关系中不正确的是
| A.ρ="(17V+22400)" /(22.4+22.4V) | B.w="17c/(1000ρ)" |
| C.w="17V/(17V+22400)" | D.C=1000Vρ/(17V+22400) |
下列原子或离子原子核外电子排布不属于基态排布的是()
| A.N:1s22s22p3 | B.S2-:1s22s22p63s23p6 |
| C.Na:1s22s22p53s2 | D.Si:1s22s22p63s23p2 |
电子排布在同一能级时,总是( )
| A.优先单独占据不同轨道,且自旋方向相同 |
| B.优先单独占据不同轨道,且自旋方向相反 |
| C.自由配对,优先占据同一轨道,且自旋方向相同 |
| D.自由配对,优先占据同一轨道,且自旋方向相反 |
下列原子的价电子排布中,对应的第一电离能最大的是( )
| A.3s23p1 | B.3s23p2 |
| C.3s23p3 | D.3s23p4 |
下列原子的电子排布图中,符合洪特规则的是( )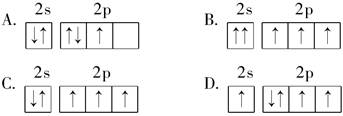
下列能级轨道数为3的是()
| A.s能级 | B.p能级 | C.d 能级 | D. f能级 |